Willkommen im Dr. Galva - Infobereich
Hier findest du Antworten auf die am häufigsten gestellten Fragen zur Galvanik. Ob du mehr über unsere Produkte oder den Bestellvorgang erfahren möchtest – auf dieser Seite findest du umfassende Informationen. Solltest du dennoch eine Frage haben, die hier nicht beantwortet wird, zögere bitte nicht, uns zu kontaktieren.
Den Leitfaden zum Galvanisieren findest du hier:
Wenn du an Informationen über die neuesten Entwicklungen oder andere Publikationen interessiert bist, dann schau dir den Bereich „Publikationen“ an: Publikationen
- Was ist der unterschied zwischen einer Brünierung und Patinierung?
-
Der Unterschied zwischen Brünierung und Patinierung liegt in den Verfahren, Materialien und Endergebnissen, obwohl beide Prozesse darauf abzielen, eine schützende oder dekorative Oberfläche auf Metall zu erzeugen:
Brünierung:
- Verfahren: Ein chemischer Prozess, bei dem Eisen oder Stahl durch Reaktion mit oxidierenden Chemikalien in eine schwarze oder dunkelblaue Schicht (Oxidschicht) umgewandelt wird.
- Materialien: Typischerweise bei Stahl und Eisen verwendet.
- Endergebnis: Erzeugt eine dunkle, matte oder leicht glänzende Oberfläche, die als Korrosionsschutz dient und gleichzeitig optisch ansprechend ist.
- Verwendung: Häufig bei Waffen, Werkzeugen oder anderen Stahlteilen, um diese zu schützen und eine dunkle Optik zu verleihen.
Patinierung:
- Verfahren: Ein chemischer oder natürlicher Prozess, bei dem Metalle wie Kupfer, Bronze oder Messing oxidieren und eine farbige Oberfläche (Patina) bilden.
- Materialien: Vorwiegend bei Kupfer, Bronze und Messing angewendet.
- Endergebnis: Erzeugt oft grüne, blaue oder braune Töne (z.B. die bekannte grüne Patina auf Kupferdächern), die meist dekorativ sind und zusätzlich als Schutzschicht dienen.
- Verwendung: Häufig in der Kunst, bei Skulpturen oder Architektur, um eine antike oder ästhetisch gealterte Oberfläche zu schaffen.
Zusammengefasst: Brünierung wird hauptsächlich bei Stahl eingesetzt, um eine dunkle, funktionale Schutzschicht zu erzeugen, während Patinierung auf Kupfer und ähnlichen Metallen angewendet wird, um eine dekorative, farbige Oberfläche zu schaffen.
- Wie kann ich Messing schwarz brünieren? Welches Produkt empfehlen Sie dafür?
-
Für das Schwarzfärben von Messing eignet sich eine Patinierung am besten. Das Patiniergel Nero ist speziell dafür entwickelt, um Messing eine dunkle Oberfläche zu verleihen. Es ist einfach anzuwenden und sorgt für eine langlebige, dekorative Patina.
Bei Verdünnung kann man auch sehr gut Brauntöne erreichen.
- Worin unterscheiden sich die Brünierungen?
-
Die Brünierungen von Dr. Galva unterscheiden sich in erster Linie durch die Art der Anwendung und die spezifischen Einsatzmöglichkeiten. Hier sind die wesentlichen Unterschiede zwischen den drei Arten:
Ultra-3 Tauchbrünierung
- Anwendung: Die Tauchbrünierung ist ideal für die Bearbeitung von mehreren Werkstücken gleichzeitig oder für komplexe Formen, die eine gleichmäßige Beschichtung erfordern. Bei dieser Methode wird das gesamte Werkstück in die Brünierungslösung eingetaucht.
- Vorteile: Diese Methode sorgt für eine gleichmäßige, durchgehende Brünierung, auch in schwer zugänglichen Bereichen. Sie ist besonders geeignet für größere Werkstücke und industrielle Anwendungen.
- Einsatzgebiete: Optimal für die Brünierung von Stahlteilen in der Massenproduktion oder in Werkstätten, wo viele Teile gleichzeitig behandelt werden müssen.
Ultra-5 Schnellbrünierung
- Anwendung: Diese Universalbrünierung ist vielseitig einsetzbar und kann sowohl im Tauchverfahren als auch durch einfaches Auftragen angewendet werden. Sie ist für eine breite Palette von Materialien und Werkstücken geeignet.
- Vorteile: Diese Brünierung bietet Flexibilität in der Anwendung und ist eine hervorragende Allround-Lösung für verschiedene Projekte. Sie ist leicht in der Handhabung und erfordert keine speziellen Ausrüstungen.
- Einsatzgebiete: Perfekt für Handwerker und Heimwerker, die eine vielseitige Lösung für verschiedene Brünierungsaufgaben suchen, sei es für kleine oder große Teile.
Ultra-7 Streichbrünierung
- Anwendung: Bei der Streichbrünierung wird die Lösung direkt auf die Oberfläche des Werkstücks aufgetragen, beispielsweise mit einem Pinsel oder Tuch. Diese Methode eignet sich besonders für die Bearbeitung von kleinen Flächen oder für Nachbesserungen.
- Vorteile: Diese Methode ermöglicht eine präzise und kontrollierte Anwendung, ideal für Reparaturen oder für Werkstücke, die nicht komplett eingetaucht werden können. Sie ist schnell und einfach anzuwenden, auch an Ort und Stelle.
- Einsatzgebiete: Geeignet für kleinere Projekte, Reparaturen oder zur Auffrischung bereits bestehender Brünierungen. Sie ist ideal für Handwerker, die gezielte Bereiche behandeln möchten, ohne das gesamte Werkstück zu bearbeiten.
Zusammenfassung:
- Tauchbrünierung: Für gleichmäßige und vollständige Beschichtungen von mehreren oder großen Werkstücken.
- Schnellbrünierung: Vielseitig einsetzbar, sowohl im Tauchverfahren als auch durch Auftragen, für verschiedene Materialien.
- Streichbrünierung: Präzise und einfache Anwendung für kleinere Flächen oder Nachbesserungen.
Jede dieser Brünierungsarten von Dr. Galva bietet spezifische Vorteile und ist für bestimmte Anwendungsbereiche optimiert, sodass Du für jede Aufgabe die richtige Methode wählen kannst.
Die Brünierungen von Dr. Galva sind speziell für Stahl, Eisen oder Gusseisen entwickelt. Es gibt auch Brünierungen, die für Legierungen wie Kupfer oder Messing geeignet sind - dies sind dann Patinierungen. - Welches Öl nach dem Brünieren?
-
Nach dem Brünieren empfiehlt sich die Verwendung eines speziellen Korrosionsschutzöls, das für brünierte Oberflächen entwickelt wurde. Hier sind einige Optionen:
-
Spezielle Brünieröle: Diese Öle sind speziell für die Versiegelung und den Schutz brünierter Oberflächen formuliert. Sie bieten einen hohen Korrosionsschutz und erhalten die schwarze Oberfläche.
-
Waffenöl: Waffenöl, wie es für die Pflege von Feuerwaffen verwendet wird, ist eine gute Wahl. Es ist darauf ausgelegt, Metalloberflächen vor Korrosion zu schützen und eignet sich daher auch hervorragend für brünierte Teile.
-
Leinöl: Für einen natürlichen Schutz eignet sich auch Leinöl, das eine dünne Schutzschicht bildet und gleichzeitig die Brünierung hervorhebt. Es ist jedoch weniger haltbar als spezialisierte Öle.
-
Mineralöl: Ein leichtes Mineralöl kann ebenfalls verwendet werden, besonders wenn kein spezielles Brünieröl zur Hand ist. Es bietet grundsätzlichen Schutz vor Feuchtigkeit, ist aber möglicherweise nicht so effektiv wie speziellere Produkte.
Wichtig ist, das Öl gleichmäßig und dünn aufzutragen, um eine gleichmäßige Schutzschicht zu gewährleisten, und überschüssiges Öl nach einigen Minuten abzuwischen, damit die Oberfläche nicht klebrig bleibt.
-
- Wie trocknen nach dem Brünieren?
-
Trockne die Teile direkt nach dem Brünieren mit einem sauberen, fusselfreien Tuch, da sich sonst Korrosion bilden kann.
Bezüglich der Wartezeit nach dem Brünieren: Es ist wichtig, dass die Brünierung vollständig abgeschlossen und die Oberfläche trocken ist, bevor Sie mit dem Lackieren beginnen. In der Regel reicht eine kurze Wartezeit von etwa 30 Minuten bis 1 Stunde aus, um sicherzustellen, dass die Oberfläche stabil ist. Sollte die Luftfeuchtigkeit hoch sein, kann es sinnvoll sein, etwas länger zu warten oder die Teile vorsichtig zu erwärmen, um den Trocknungsprozess zu beschleunigen.
- Ist ein Ölen der brünierten Teile auch notwendig wenn diese danach lackiert werden?
-
Die Ölung der brünierten Teile dient primär dem zusätzlichen Korrosionsschutz, indem sie die Oberfläche versiegelt und vor Feuchtigkeit schützt. Wenn Sie die brünierten Metallbleche jedoch anschließend mit Klarlack lackieren möchten, kann das Ölen in der Tat entfallen, da der Klarlack die schützende Schicht übernimmt.
Außerdem würde der Lack dann nicht haften.
- Wie stark ist der Korrosionsschutz einer Brünierung?
-
Der Korrosionsschutz einer Brünierung ist begrenzt und bietet in der Regel nur einen moderaten Schutz vor Rost. Die Schnellbrünierung erzeugt eine dünne, schwarze Oxidschicht auf der Oberfläche des Metalls, die in gewissem Maße vor Korrosion schützt, jedoch nicht so wirksam ist wie eine dickere, industrielle Brünierung oder eine Beschichtung.
Faktoren, die den Korrosionsschutz beeinflussen:
-
Dicke der Schicht: Da die Oxidschicht, die durch Brünierung entsteht, relativ dünn ist, bietet sie nur einen oberflächlichen Schutz.
-
Umgebungsbedingungen: In feuchten oder aggressiven Umgebungen, wie in salzhaltiger Luft, ist der Schutz durch eine Brünierung oft unzureichend und kann relativ schnell versagen, wenn die Oberfläche nicht zusätzlich behandelt wird.
-
Nachbehandlung: Der Korrosionsschutz kann deutlich verbessert werden, wenn die brünierte Oberfläche nach der Anwendung mit einem geeigneten Korrosionsschutzöl behandelt wird. Diese Nachbehandlung versiegelt die Oberfläche und schützt sie vor Feuchtigkeit und anderen korrosiven Einflüssen.
Zusammenfassung:
Ohne Nachbehandlung bietet die Brünierung nur einen eingeschränkten Korrosionsschutz und ist hauptsächlich für dekorative oder temporäre Anwendungen geeignet. Für langfristigen Schutz, insbesondere in anspruchsvollen Umgebungen, ist eine Nachbehandlung mit Öl oder einer anderen Schutzbeschichtung erforderlich.
-
- Stabanode oder Flachanode – welche ist die Richtige?
-
Die Entscheidung zwischen einer Stabanode oder einer Flachanode hängt von mehreren Faktoren ab:
1. Werkstückgröße und Form
- Flachanode: Ideal für größere Werkstücke oder wenn eine gleichmäßige Schichtdicke über eine größere Fläche gewünscht ist. Perfekt für die Badgalvanik.
- Stabanode: Besser für kleinere Werkstücke oder wenn die Beschichtung auf bestimmte Bereiche konzentriert werden soll. Perfekt für die Stiftgalvanik.
2. Stromverteilung
- Flachanode: Sorgt für eine gleichmäßigere Stromverteilung, da sie über eine größere Oberfläche verfügt – ideal für gleichmäßige Beschichtungen.
- Stabanode: Kann zu ungleichmäßiger Abscheidung führen, insbesondere wenn der Abstand zur Kathode nicht konstant bleibt. In der Badgalvanik kann dies zu einer zu hohen anodischen Stromdichte führen.
3. Anordnung der Elektroden
- Flachanode: Eine symmetrische Anordnung mit zwei gegenüberliegenden Flachanoden ermöglicht eine gleichmäßige Metallabscheidung.
- Stabanode: Sollte so positioniert werden, dass der Abstand zum Werkstück möglichst konstant bleibt, um Schichtdickenunterschiede zu vermeiden. Strom fließt immer auf dem kürzesten Weg!
4. Stabanode für Stiftgalvanik
- Eine Stabanode kommt vor allem in der Stiftgalvanik (auch Tampongalvanik genannt) zum Einsatz, da sie eine präzise Beschichtung ermöglicht.
- Ideal zum Nachbessern kleiner Bereiche oder für Werkstücke, die nicht vollständig in ein Galvanikbad getaucht werden können.
5. Flachanode für die Badgalvanik
- Flachanoden sind besonders vorteilhaft für die Badgalvanik, da sie eine gleichmäßige Metallabscheidung auf größeren Werkstücken gewährleisten.
- In einem Galvanikbad wird das Werkstück von mehreren Seiten umspült, was für eine homogene Schicht sorgt.
- Zwei gegenüberliegende Flachanoden sorgen für eine symmetrische Stromverteilung und verbessern die Schichtqualität erheblich.
Fazit
- Für eine gleichmäßige Schichtdicke und größere Werkstücke → Flachanode, besonders bei Badgalvanik.
- Für kleinere oder gezielte Beschichtungen → Stabanode, besonders bei Stiftgalvanik.
- Berücksichtige immer die Eigenschaften des Elektrolyten und die Stromverteilung!
- Was benötige ich zum Galvanisieren?
-
1. Stromquelle
- Eine regelbare Gleichspannungsquelle (Netzteil) mit passender Spannung und Stromstärke für den jeweiligen Elektrolyten.
2. Elektrolytlösung
- Eine spezielle Elektrolytlösung, die Metallionen enthält (z. B. Kupferelektrolyt für Kupferabscheidung, Nickelelektrolyt für Nickelbeschichtung).
3. Anode (Pluspol, +)
- Kupferanode für Kupferbeschichtung
- Nickelanode für Nickelbeschichtung
- Zinkanode für Zinkelektrolyt
- Aluminiumanode für Chromelektrolyt (alternativ Platinanode)
- Edelstahl- oder Platinanode für Edelmetalle oder bestimmte Spezialelektrolyte
4. Kathode (Minuspol, -)
- Das Werkstück, das beschichtet werden soll (z. B. Metallteile, Schmuckstücke).
5. Behälter
- Eine Wanne oder ein Kunststoffbehälter (chemikalienbeständig) für das Galvanikbad.
6. Leitungsdrähte und Klemmen
- Krokodilklemmen und Kabel zur Verbindung der Elektroden mit der Stromquelle.
7. Vor- und Nachbehandlungsmittel
- Reinigungsmittel & Aktivatoren (z. B. Entfetter, Beizlösungen – dazu gehört der Konditionierer).
- Passivierung & Schutzmittel (z. B. Brünieröl), um die Schicht zu schützen.
8. Schutzausrüstung
- Handschuhe, Schutzbrille und ggf. Atemschutz, um mit Chemikalien sicher zu arbeiten.
- Welches Set bzw. Netzteil sollte ich nehmen?
-
Zuerst sollte entschieden werden, was man erreichen will, also welche Schicht man final aufbauen will.
Die Optionen sind Chrom, Kupfer, Nickel und Zink.
Zusätzlich gibt es noch Kombis aus Kupfer/Nickel, Chrom/Nickel und das Große Set.
Das Set für Chrom gibt es nur als Chrom/Nickel-Kombi, da vor dem Verchromen generell vernickelt werden sollte und das Chrom darauf nur dünn abgeschieden wird.
Kupfer unter Nickel ist oft vorteilhaft, da der Korrosionsschutz stark verbessert wird; sowie wenn Unebenheiten ausgeglichen werden sollen; oder poliert werden soll.
Das große Set ist sehr gut geeignet, wenn man alles machen möchte.
Natürlich kann man auch jedes Set später anders nutzen, man muss nur die Elektrolyte und Anoden ergänzen, schon lässt sich eine andere Schicht auftragen.
Als Nächstes ist die Frage welches Netzteil benötigt wird. Hier haben wir ein kleines mit max. 3A und ein starkes mit 10A.
Hierbei entscheidet man, wie groß der zu beschichtende Gegenstand sein soll. Möchte man später etwas Größeres beschichten ist ein starkes Netzteil nötig (10A). Später braucht man sich einfach nur größere Wannen zulegen und darin beschichten (und natürlich auch Elektrolyte).
Generell arbeitet man in der Galvanik mit der Stromdichte, da jeder Elektrolyt seinen eigenen optimalen Bereich hat. Diese wird in A/dm² angegeben.
Um die benötigte Stromstärke zu berechnen, multiplizierst du die empfohlene Stromdichte für den jeweiligen Elektrolyten mit der Oberfläche des Werkstücks in dm². Die Spannung passt sich automatisch an, sobald die Stromstärke mittels der Strombegrenzung entsprechend eingestellt wurde (die Spannung wird automatisch reduziert, bis der gewählte Strom erreicht wird).
In dieser Tabelle kannst du die benötigte Leistung ablesen, welche benötigt wird.
Elektrolyt Ausgangsstrom 3A* 5A* 10A* Chrom 0,6 1 2 Kupfer sauer 5 8,5 17 Kupfer alkalisch 15 25 50 Nickel 10 17 34 Zink 12 20 40 Zink-Nickel 3,3 5,5 11 * - Angaben der maximal zu beschichtenden Fläche in dm² bei kleinstmöglicher Stromdichte
- Was ist Galvanik?
-
Galvanik, auch bekannt als Elektroplattieren, ist ein elektrochemischer Prozess, bei dem eine dünne Metallschicht auf ein anderes Material aufgebracht wird. Dieser Prozess wird oft verwendet, um die Oberfläche eines Objekts zu veredeln, vor Korrosion zu schützen, die Verschleißfestigkeit zu erhöhen oder um das Aussehen zu verbessern.
So funktioniert die Galvanik:
-
Vorbereitung des Werkstücks: Das Werkstück, das beschichtet werden soll, muss gründlich gereinigt werden, um Verunreinigungen wie Öl, Fett oder Rost zu entfernen. Dies ist entscheidend für die Haftung der Metallschicht.
-
Elektrolytbad: Das Werkstück wird in ein Elektrolytbad getaucht, das eine Lösung von Metallionen enthält, die auf das Werkstück abgeschieden werden sollen. Das Werkstück wird dabei als Kathode (negativ geladen) und eine Metallanode (positiv geladen) als Quelle der Metallionen verwendet.
-
Anwendung von elektrischem Strom: Ein elektrischer Strom wird durch das Elektrolytbad geleitet. Dabei bewegen sich die positiv geladenen Metallionen zur negativ geladenen Kathode, wo sie sich als feste Metallschicht abscheiden. Die Dicke und Qualität der Metallschicht können durch die Stärke des Stroms, die Zusammensetzung des Elektrolyten und die Dauer des Prozesses gesteuert werden.
-
Abschluss: Nach dem Beschichtungsprozess wird das Werkstück gereinigt und gegebenenfalls poliert, um das gewünschte Finish zu erzielen.
Anwendungen der Galvanik:
- Korrosionsschutz: Metalle wie Zink oder Nickel werden auf Stahl aufgebracht, um Rostbildung zu verhindern.
- Dekorative Beschichtung: Edelmetalle wie Gold oder Silber werden auf Schmuck oder dekorative Gegenstände aufgebracht, um deren Aussehen zu verbessern.
- Verschleißschutz: Härtere Metalle wie Chrom werden auf Werkzeuge oder Maschinenteile aufgebracht, um deren Lebensdauer zu verlängern.
- Elektronische Anwendungen: In der Elektronik werden dünne Metallschichten auf Leiterplatten oder Kontakte aufgebracht, um die elektrische Leitfähigkeit zu verbessern.
Die Galvanik ist eine weit verbreitete Technik in der Industrie und im Handwerk und spielt eine wichtige Rolle in zahlreichen Produktionsprozessen.
-
- Die Verfahren der Galvanotechnik
-
Im folgenden Abschnitt werden die verschiedenen Verfahren der Galvanotechnik vorgestellt, wobei auch auf die grundlegenden Arbeitsutensilien für die einzelnen Methoden eingegangen wird. Im Allgemeinen wird zwischen drei verschiedenen galvanischen Verfahren unterschieden, nämlich der Trommelgalvanik, der Stift-/Tampongalvanik und der Badgalvanik.
Die Verfahren im Überblick
Man unterscheidet zwischen 3 Verfahren zum galvanischen Abscheiden von Metallen. Das sind die Badgalvanik, die Stiftgalvanik (oder auch Tampongalvanik), sowie die Trommelgalvanik. Jedes dieser Verfahren hat seine Vorteile und Nachteile.
Verfahren Vorteile Nachteile Badgalvanik - Automatischer Ablauf des Galvanisierungsprozesses
- Schichtdicken von wenigen Mikrometern bis mehreren Millimetern erzielbar
- Starkes Netzteil nötig
- Große Behälter notwendig
- Große Menge an Elektrolyt
- Unpraktikabel für das Galvanisieren von kleinen Teilen
Stiftgalvanik / Tampongalvanik - Galvanisieren großer Flächen durchführbar
- Netzteil mit schwacher Leistung notwendig, denn Strom fließt nur an kleiner Kontaktstelle
- Geringe Menge an Elektrolyt nötig
- Nur geringe Schichtdicken erreichbar, dadurch kaum Korrosionsschutz
- Galvanisierungsprozess läuft nicht automatisiert ab
- Sehr zeitaufwendig
- Anstrengend
Trommelgalvanik - Hervorragend geeignet zum Galvanisieren von Kleinteilen
- Aufgrund kontinuierlicher Rotation relativ gleichmäßige Beschichtung
- Galvanisierungsprozess läuft automatisch ab
- Schnell zu befüllen
- Starkes Netzteil notwendig
- Große Behälter unerlässlich
- Große Menge an Elektrolyt
- Werkstücke erhalten kleine Schlagstellen
- Gewisse Stückzahl nötig, damit die Werkstücke dauerhaft kontaktiert werden, bzw. geeignete Trommelgröße
Das Verfahren der Badgalvanik
Bei der Badgalvanik handelt es sich um eine Methode, bei der das zu galvanisierende Werkstück und die Anode in einen Elektrolyt getaucht werden. Zudem wird ein Stromfluss erzeugt, so dass es zur Metallabscheidung auf dem Werkstück kommt.
Bei der Badgalvanik handelt es sich um ein in der Industrie häufig genutztes Verfahren. In der Regel werden Werkstücke in Wannen enormer Größe verchromt, vergoldet oder vernickelt. Dafür kommen oft Gestelle zur Anwendung auf denen die zu beschichtenden Teile aufgehängt werden. Zur Erhöhung der möglichen Stromdichte und damit schnelleren Abscheiden bietet sich hier eine Badbewegung an. Dies kann durch Lufteinblasung, Pumpen oder auch Bewegung des Gestells erfolgen.
Vorteilhaft ist, dass das Verfahren leicht durchzuführen ist und große Stromflüsse erzeugt werden können, so dass auch eine Abscheidung dicker Metallschichten möglich ist. Nachteilig ist, dass hohe Elektrolytmengen zum Befüllen der Wannen notwendig sind. Aus diesem Grund eignet sich die Badgalvanik für den Privat- bzw. Hobbybereich nur für kleinere Teile.
Benötigte Grundausstattung
Zur Durchführung des Verfahrens der Badgalvanik sind eine regelbare Gleichstromquelle, eine Wanne bzw. ein Behälter, Verbindungskabel notwendig.
Bei der Stromquelle kann es sich zum Beispiel um ein Labornetzgerät handeln, wobei sowohl eine Volt- als auch Ampere-Anzeige, d.h. Spannung und Strom, vorhanden sein sollte. Der Behälter sollte so groß sein, dass das zu galvanisierende Objekt komplett eingetaucht werden kann. Er sollte aus einem alkalibeständigen und säurebeständigen Material bestehen; neben Kunststoffbehältern eignen sich auch Glasbehälter sehr gut. Zudem benötigen sie Kabel, um die Stromversorgung sowohl an die Anode als auch an das Werkstück anzuschließen. Um Verwechslungen zu vermeiden, verwenden Sie immer ein rotes Kabel für den (+) Pol und ein schwarzes Kabel für den (-)-Pol.
Anodenfläche
Grundsätzlich gilt: Die Fläche der Anode sollte möglichst die Oberflächengröße des zu galvanisierenden Werkstücks besitzen. Sollte die Anodenfläche hingegen eine zu kleine Oberfläche aufweisen, ist es möglich, dass die Schichten ungleichmäßig abgeschieden werden.
Dieser Effekt entsteht, da der Strom sich nicht gleichmäßig im Elektrolyt verteilt (Streuung) und dieser den kürzesten Weg nimmt. So ist im Bereich des kürzesten Weges der Strom höher und die Schicht scheidet hier dicker ab. Auch die Anodenform und Anordnung muss geeignet sein, dass sich der Strom gleichmäßig verteilen kann.
Eine größere Anode wirkt sich nicht negativ auf das Ergebnis aus. Allerdings kann aufgrund einer ungünstigen anodischen Stromdichte (anodischer Wirkungsgrad) eine stärkere Passivierung (abhängig vom Elektrolyt) stattfinden, wodurch der Stromfluss reduziert wird. Ist dies der Fall sollte die Anode gereinigt werden.
Das Verfahren der Stift- bzw. Tampongalvanik
Sollen fest montierte oder große Werkstücke galvanisiert werden, eignet sich die Stiftgalvanik am besten. Hierzu nutzt man einen als Anode (+) geschalteten Metallstab an dessen Spitze sich entweder ein Tampon aus Stoff oder ein Schwamm befindet (zur Vereinfachung nutzen wir nur das Wort Tampon). Der Tampon dient zur Aufnahme des Elektrolyts und wird mit dem gewünschten Elektrolyt komplett vollgesogen. Während das zu galvanisierende Objekt mit der Kathode (-) verbunden ist, wird das Werkstück mit dem Tampon nun in kreisender Bewegung kontaktiert. Auf diese Weise wird ein Stromfluss ermöglicht und nach wenigen Sekunden scheidet sich an den entsprechenden Kontaktstellen eine Metallschicht ab.
Die kreisende Bewegung ist sehr wichtig, da auf einer kleinen Kontaktfläche ein hoher Strom fließt. Sobald man mit dem Tampon auf einer Stelle stehen bleibt, kann die Stelle matt werden und kann sich dunkel verfärben (Anbrennungen), dieser Effekt läuft schneller ab, je höher der Stromfluss ist. Hier ist also ein bisschen Erfahrung nötig, die man aber recht schnell bekommt. Ein Hin- und Herbewegen des Tampons ist eher ungeeignet, da zwischendurch die Bewegung kurzzeitig unterbrochen wird und bei hoher Stromdichte bereits Anbrennungen stattfinden können.
Bevorzugt sollte die Anode vorrangig aus inerten Materialien wie zum Beispiel Platin oder Grafit (sowie teilweise auch Edelstahl) oder aber demjenigen Material des eingesetzten Elektrolyten bestehen.
Benötigte Grundausstattung
Zur Durchführung des Verfahrens der Stift- oder Tampongalvanik bzw. Stiftgalvanik werden eine regelbare Gleichstromquelle, d.h. ein regelbares Netzteil mit digitaler Spannungs- und Stromanzeige, eine Stiftanode mit Anodenhalter (Galvanikstift), ein Kabelsatz sowie ein Tampon oder Schwamm benötigt. Die Stiftanode (bzw. die Anodenhalterung) muss am (+)-Pol des Netzteils mithilfe eines Kabels angeschlossen werden. Zudem gilt es die Anode mit einem Tampon oder Schwamm zu bestücken, so dass der vollständige Galvanikstift einsatzbereit ist. Das Werkstück selbst wird wie bei den weiter oben erläuterten Verfahren an den (-)-Pol angeschlossen.
Schwamm & Tampon
Kommen Schwämme oder Tampons zum Einsatz, handelt es sich um Aufsätze, die den Elektrolyt aufsaugen. Diese Charakteristik ist unerlässlich, da er der Elektrolyt während des Galvanisierungsverfahrens zwischen Anode und Werkstück gehalten werden muss und die Metallionen abgeben muss. Idealerweise verfügen Tampon-Aufsätze zum Galvanisieren über eine sehr hohe Saugfähigkeit und sind robust. Galvanik-Tampons sollten auch nicht zu dünn sein, denn sonst könnte es zu Isolationseffekten durch punktuell hohen Druck kommen und der elektrische Strom nicht weitergeleitet werden. Auch äußerliche Nahtstellen sollte ein Tampon zum Galvanisieren nicht besitzen, da hierdurch Kratzer auf dem Metall entstehen könnten.
Eindicker respektive Gelbildner
Bei einem Eindicker, der auch als Gelbildner bezeichnet wird, handelt es sich um ein spezifisches Verdickungsmittel. Eindicker werden zur Elektrolytlösung hinzugefügt, so dass diese dickflüssiger wird. Es gibt spezielle Eindicker, die für die verschiedenen galvanischen Elektrolyte konzipiert wurden. Werden herkömmliche Mittel verwendet bzw. untergemischt, wird das Elektrolyt in der Regel unbrauchbar. Mithilfe galvanischer Gelbildner können grundsätzlich alle Arten der Elektrolyte eingedickt werden. Durch das Eindicken des Elektrolyten wird sichergestellt, dass die Flüssigkeit nicht tropft, sauberer gearbeitet werden und sparsam mit Elektrolyt umgegangen werden kann. Allerdings sollte der Elektrolyt nicht zu dickflüssig sein.
Um einen Elektrolyten einzudicken, sollten Sie so viel Elektrolyt, wie Sie voraussichtlich benötigen in einen Behälter füllen und unter gleichmäßigem Rühren so viel Gelbildner hinzufügen, bis die individuell gewünschte Konsistenz resp. Festigkeit erreicht ist. Gehen Sie hierbei sorgsam und langsam vor. Achten Sie unbedingt darauf, dass es bei der Verwendung von Pulver nicht zu einer zu starken Staubentwicklung kommt. Sollten Sie das Elektrolyt zu stark eingedickt haben, können Sie es durch Zugabe von unverdicktem Elektrolyt wieder flüssiger machen.
Das Verfahren der Trommelgalvanik
Zum Galvanisieren von großen Mengen an Kleinteilen ist das Verfahren der Trommelgalvanik ideal geeignet, ins besonders für Teile, die nicht oder nur mit großem Aufwand auf Gestellen befestigt werden können. Grundsätzlich entspricht der Galvanisierungsprozess demjenigen der Badgalvanik, wobei die zu galvanisierenden Werkstücke sich lose in einer langsam rotierenden Trommel befinden. Kontaktiert werden die Werkstücke mithilfe einer mittig angebrachten Kontaktstange, frei bewegliche Klöppel (Kabel mit leitfähiger Kappe) oder über geeignete Kontaktpunkte in der Trommelwand; die Trommel wird mithilfe eines Motors in Rotation versetzt. Die hierdurch entstehende gleichmäßige Bewegung stellt eine relativ gleichmäßige Beschichtung der Kleinteile sicher, allerdings bestehen feine Unterschiede, da durch die unkontrollierte Durchmischung einzelne Teile länger kontaktiert werden und somit eine höhere Schichtdicke erhalten, bzw. dieser Effekt auch umgekehrt erfolgt (also geringere Kontaktzeit und geringere Schichtdicke).
Vorteilhaft ist hier, dass es schnell zu beladen ist, da die Teile einfach lose hineingegeben werden. Nachteilig ist, dass die Werkstücke immer kleine Schlagstellen erhalten, da sie untereinander durchmischt werden, daher ist dieser Prozess weniger für Spiegelglanz geeignet, was aber bei Schrauben etc. keine Rolle spielt. Auch ist eine Mindeststückzahl nötig, dass die Teile durchgängig kontaktiert werden.
Benötigte Grundausstattung
Zum Durchführen des Trommelgalvanikverfahrens benötigen Sie eine Galvaniktrommel. Neben einer Trommel sind ein Getriebemotor sowie die Mechanik die grundlegenden Komponenten, zusammen ist dies eine Trommelgalvanikanlage. Ebenso wie für das Verfahren der Badgalvanik werden ein ausreichend starkes regelbares Netzgerät und ein Kabelsatz notwendig.
Das Befüllen der Galvaniktrommel
Grundsätzlich gilt: Die Galvaniktrommel sollte maximal bis zu einer Auslastung zwischen 40 und 50 Prozent mit Werkstücken befüllt werden. Hierdurch wird sichergestellt, dass die Komponenten frei beweglich sind; zugleich wird einem Verklemmen, Verkanten oder sogar Blockieren vorgebeugt. Würde dies passieren, könnte aufgrund der Kontaktstellen keine ideale Beschichtung und damit gleichmäßige Galvanisierung stattfinden. Unbedingt darauf achten, dass diese auch Kontakt zum Kontaktstift haben.
Hinweis: Bei Kugeln handelt es sich um das optimale Füllmaterial, denn sie können nicht verkanten, eine freie Bewegung ist ebenso sichergestellt wie ein ideales Galvanisierungsergebnis.
- Wie verhält sich das mit der Spannung und Stromdichte?
-
In der Galvanik spielen Spannung und Stromdichte eine entscheidende Rolle für die Qualität der abgeschiedenen Schicht. Beide Parameter müssen sorgfältig eingestellt werden, um eine gleichmäßige und hochwertige Metallbeschichtung zu erzielen.
1. Spannung:
- Funktion: Die Spannung (gemessen in Volt) treibt den elektrischen Strom durch den Elektrolyten, der die Metallionen von der Anode zur Kathode (dem Werkstück) transportiert, wo sie sich als Metallbeschichtung absetzen.
- Einfluss: Eine zu hohe Spannung kann dazu führen, dass die Metallionen zu schnell abgeschieden werden, was eine raue, poröse oder sogar pulverige Schicht erzeugen kann. Eine zu niedrige Spannung kann hingegen dazu führen, dass die Abscheidung zu langsam verläuft, was die Effizienz des Prozesses verringert und zu einer ungleichmäßigen Schicht führt.
- Abhängigkeit von der Entfernung: Die Spannung muss entsprechend der Entfernung zwischen Anode und Kathode angepasst werden, da der elektrische Widerstand des Elektrolyten mit der Distanz zunimmt. Je weiter die Anode von der Kathode entfernt ist, desto höher muss die Spannung eingestellt werden, um eine ausreichende Stromdichte zu erreichen. Die Spannungsangaben auf unseren Elektrolyten sind als Richtwerte zu verstehen und beziehen sich auf einen Abstand von etwa 10 cm. Wenn dieser Abstand variiert, sollte auch die Spannung entsprechend angepasst werden.
- Maximalwerte: Beachte, dass die angegebenen Maximalwerte für die Spannung oft nur unter idealen Bedingungen erreicht werden können, beispielsweise bei Verwendung einer Badbewegung (z. B. durch Rühren oder Pumpen), die den Elektrolyten gleichmäßig um das Werkstück zirkulieren lässt und so Hotspots oder ungleichmäßige Abscheidungen verhindert.
2. Stromdichte:
- Definition: Die Stromdichte ist der Strom, bezogen auf die Fläche der Elektrode, und wird in Ampere pro Quadratdezimeter (A/dm²) angegeben. Sie beschreibt das Verhältnis zwischen dem elektrischen Strom und der Elektrodenoberfläche und ist ein entscheidender Faktor für die Qualität der Metallabscheidung.
- Einfluss auf die Kathode (Werkstück): Die kathodische Stromdichte beeinflusst maßgeblich die Qualität der Beschichtung auf dem Werkstück (Kathode). Bei jedem Elektrolyten gibt es einen optimalen Stromdichtebereich, innerhalb dessen die Abscheidung mit guten Ergebnissen erfolgt. Eine zu hohe Stromdichte kann zu rauen, grobkörnigen Schichten führen, während eine zu niedrige Stromdichte zu unzureichenden oder ungleichmäßigen Überzügen führen kann.
- Einfluss auf die Anode: Die anodische Stromdichte ist für die Stabilität des Elektrolyten entscheidend. Idealerweise sollte sich das Metall an der Anode (in der Regel das gleiche Metall, das abgeschieden wird) genauso schnell lösen, wie es an der Kathode abgeschieden wird. Dies gewährleistet eine gleichmäßige Metallionenkonzentration im Elektrolyten und trägt zur Langlebigkeit des Bades bei. In der Praxis gibt es jedoch oft Abweichungen, was die Stabilität des Elektrolyten und die Effizienz des Prozesses beeinträchtigen kann.
- Anpassung durch Temperatur und Bewegung: Höhere Stromdichten können durch das Erhöhen der Temperatur und durch die Bewegung des Elektrolyten oder des Werkstücks angewendet werden. Diese Maßnahmen verbessern den Ionentransport und helfen, die Abscheidung gleichmäßiger und effektiver zu gestalten.
- Abhängigkeit von Werkstück und Anodenform: Die Stromdichte variiert auch abhängig von der Form des Werkstücks und der Anode. Da der Strom bevorzugt den kürzesten Weg nimmt, kann eine ungleichmäßige Stromverteilung zu ungleichmäßigen Beschichtungen führen, insbesondere an Ecken, Kanten oder komplexen Geometrien. Eine sorgfältige Anpassung der Anode an das Werkstück sowie die Verwendung von Hilfselektroden kann hier Abhilfe schaffen.
- Optimierung: Eine sorgfältige Anpassung der Anode an die Form des Werkstücks sowie die Verwendung von Hilfselektroden kann helfen, eine gleichmäßige Stromverteilung zu erreichen und damit eine homogene Beschichtung sicherzustellen.
Wechselwirkungen zwischen Spannung und Stromdichte:
- Die Spannung und die Stromdichte sind miteinander verbunden: Eine höhere Spannung führt in der Regel zu einer höheren Stromdichte, sofern die Widerstände im System (wie Elektrolytwiderstand und Oberflächenbeschaffenheit) konstant bleiben.
- Eine Anpassung der Spannung ist oft erforderlich, um die gewünschte Stromdichte zu erreichen, aber auch andere Faktoren wie die Elektrolytkonzentration und Temperatur beeinflussen das Zusammenspiel.
Zusammenfassung:
- Spannung treibt den Prozess an und beeinflusst die Geschwindigkeit der Metallabscheidung. Sie muss sorgfältig eingestellt werden, insbesondere unter Berücksichtigung der Entfernung zwischen Anode und Kathode, um eine gleichmäßige Beschichtung zu erzielen.
-
Stromdichte bestimmt die Menge des abgeschiedenen Metalls pro Flächeneinheit und beeinflusst die Qualität und das Aussehen der Beschichtung. Sie muss sorgfältig auf den optimalen Bereich abgestimmt werden, um eine hochwertige Beschichtung zu erzielen.
- Sowohl die kathodische als auch die anodische Stromdichte spielen eine entscheidende Rolle: Die kathodische Stromdichte beeinflusst die Schichtqualität, während die anodische Stromdichte die Stabilität des Elektrolyten sichert. Temperatur- und Bewegungsmanagement im Bad können helfen, höhere Stromdichten zu ermöglichen und die Prozessstabilität zu verbessern.
- Eigenschaften der einzelnen Schichten
-
Jede der aufgebrachten Schichten bietet bestimmte Eigenschaften, die sich schlussendlich positiv auf die Qualität des Endergebnisses auswirken. Obwohl die Beschichtung mit Kupfer bei vielen Materialien nicht zwingend erforderlich ist, führt sie zu einem qualitativ besseren Ergebnis.
Kupfer scheidet schnell ab und sorgt für eine besonders glatte Oberfläche. Zudem ist es sehr gut zu polieren, wodurch sich die Polierkosten spürbar reduzieren. Nickel erhöht die Korrosionsbeständigkeit der gesamten Beschichtung. Bei einer anschließenden Verchromung trägt es maßgeblich zum Glanz der Chromschicht bei.
Den Abschluss bildet die dünn aufgebrachte letzte Schicht mit dem gewünschten dekorativen oder technischen Nutzen.
- Korrosionsschutz der Schichten
-
Ein guter Korrosionsschutz wird erst durch eine ausreichend dicke Schicht oder aber auch durch eine entsprechende Schichtkombination erreicht. Eine dünne Chromschicht auf Eisen wird nahezu keinen Schutz bieten, daher verwendet man mindestens die Kombination Nickel-Chrom. Einen weiteren Vorteil bietet die darunterliegende Nickelschicht, denn durch das Nickel (Glanznickel) kommt der Glanz besser zur Geltung. Falls man nun auch den Korrosionsschutz in einer reduzierenden Atmosphäre verbessern will, verwendet man die Schichtkombination Kupfer-Nickel-Chrom, da das Kupfer hier bessere Arbeit leistet.
Generell gilt also:
Abhängig des gebildeten Metalls ist der Korrosionsschutz sehr verschieden. Auch je nach unterschiedlichen Typen der Elektrolyte gibt es große Unterschiede. Recht viele Typen scheiden mit mikroskopisch feinen Poren ab – in diesen Bereichen ist der Schutz nicht vorhanden. Um die Poren zu schließen sind höhere Schichtdicken nötig. Eine Kombination mehrerer Schichten verbessert den Schutz deutlich. Die verschiedenen Schichten ergänzen sich dabei und der Korrosionsschutz steigt exponentiell an, getreu dem Motto „1+1=5“.
Beipiele zum Korrosionsschutz
Nickel:
Eine reine Nickelschicht besitzt erst einen guten Korrosionsschutz ab 25µm, aber in der Schichtkombination Nickel-Chrom oder auch Kupfer-Nickel-Chrom wird der Schutz stark verbessert.
Zink:
Für Zink empfiehlt sich eine Schichtdicke um die 10µm. Zink weist eine Fernwirkung auf, durch welche auch unbedeckte Eisenstellen (z.B. Poren oder mechanisch beschädigte Stellen) kathodisch schützt.
Zink-Nickel:
Hier trifft die Kombination aus 2 schützenden Elementen zusammen. Zum einen das aktive Zink und das passive Nickel. Beide Elemente bilden eine gemeinsame Schicht mit erhöhten Schutz. Die durchschnittlichen Schichtstärken liegen zwischen 5µm und 10µm. Die Schichten sind auch bei Temperaturen von bis zu 180°C korrosionsbeständig, weshalb sich Zink-Nickel-Schichten ideal zum Schutz von Komponenten von Verbrennungsmotoren eignen.
Hier im Beispiel ein verchromtes Gestell, mit einer offensichtlich unzureichenden Schichtdicke, bzw. ungeeigneter Ausführung der Grundschicht:

- Reihenfolge der Beschichtung
-
Die Beschichtung eines Werkstücks erfolgt im Normalfall in mehreren Schritten, wobei unterschiedliche Schichten auf die Oberfläche des Gegenstands abgeschieden werden. Jede dieser Schichten besitzt wichtige Eigenschaften für ein professionelles Ergebnis.
Abhängig vom Material und vom Zustand der Oberfläche ist eine Vorbehandlung erforderlich. So benötigen beispielsweise säureempfindliche Materialien wie Zink vor der Beschichtung mit saurem Kupferelektrolyt eine mit alkalischem Kupferelektrolyt aufgebrachte Schicht. Aluminium wird mit Aluminiumaktivator vorbehandelt und Kupfer benötigt vor dem stromlosen Aufbringen der Nickelschicht eine dünne Schicht Palladium.
Praktischer Aufbau der Schichtreihenfolge nach der Vorbehandlung:
- Glanzkupfer für eine gute Einebnung
- Nickel als Diffusionssperrschicht
- Gold, Silber oder Chrom als abschließende Schicht
Die letzte Schicht wird im Normalfall nur dünn aufgetragen.
- Die Streuung in der Galvanik
-
Hier gehen wir auf die sehr wichtige zu beachtende Streuung ein. Die Anode sollte an die Form des zu beschichtenden Werkstücks angepasst werden. Nur mehr Stromfluss alleine würde es an Stellen, welche näher zur Anode liegen, dunkel und matt werden lassen, da dann lokal die Stromdichte zu hoch wäre.
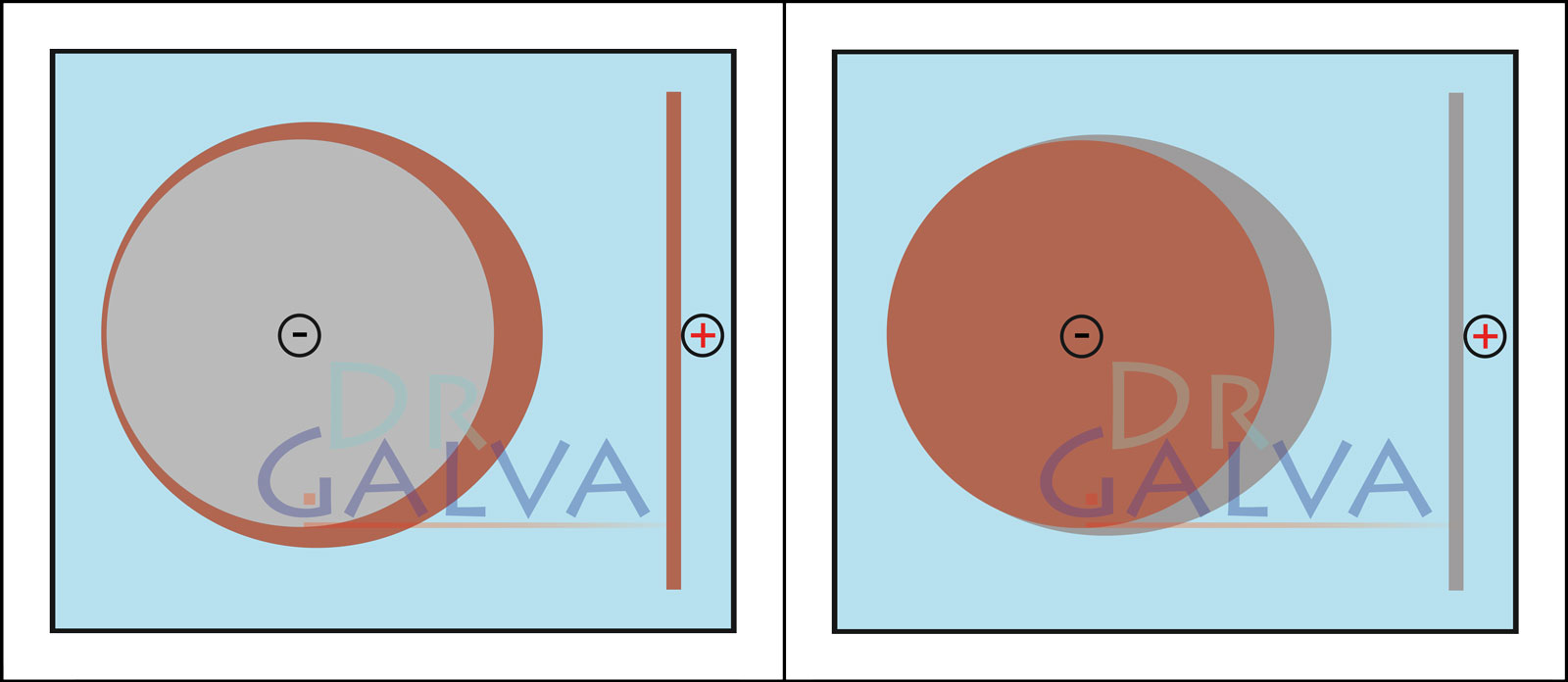
Gute Streuung (z.B. Kupfer sauer) bei Verwendung einer Flachanode. Je geringer der Abstand, desto mehr Strom fließ an diesen Stellen und mehr Metall wird dort abgeschieden. Durch die gute Streuung wird auf der Rückseite dennoch eine dünne Schicht abgeschieden. Schlechte Streuung (z.B. Zink schwach sauer). Hier wird nur auf der zur Anode zugewandten Seite Metall abgeschieden. Auf der Rückseite fließt praktisch kein Strom und es erfolgt dort keine Abscheidung, bzw. nur minimal. 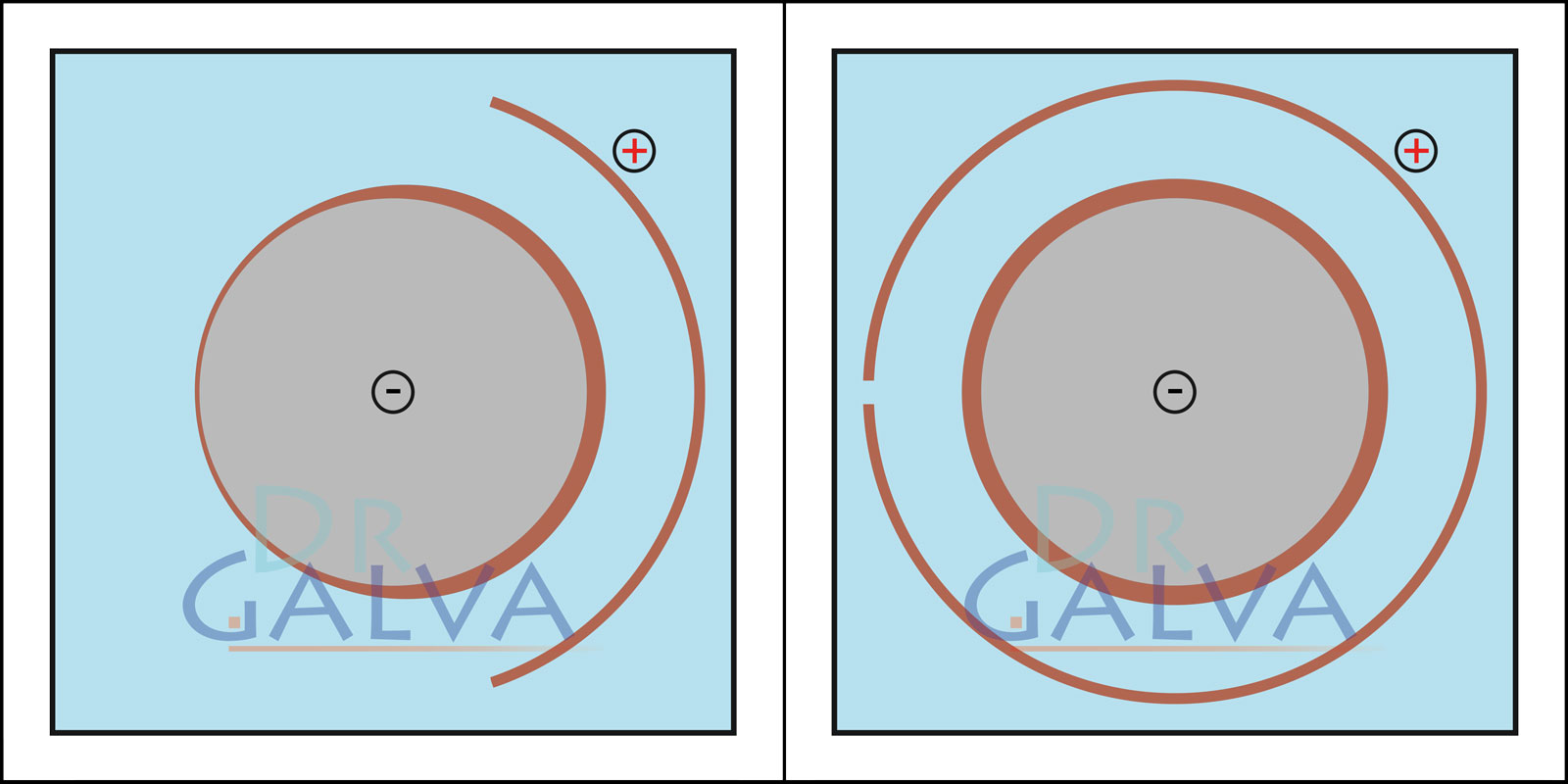
Bei einer an das Werkstück angepassten Form scheidet das Metall deutlich gleichmäßiger ab. Auf der Anode abgewandten Seite wird die Schicht dünner. Insgesamt wird die Schicht deutlich gleichmäßiger im Vergleich zu einer Flachanode. Im galvanischen Bad sind eine Ringanode und das Werkstück zu finden. Auf diese Weise wird sichergestellt, dass der Anodenabstand zum Werkstück rundherum gleichgroß ist. Um eine gleichmäßige Abscheidung zu erreichen, ist es nicht notwendig, das Werkstück zu drehen. 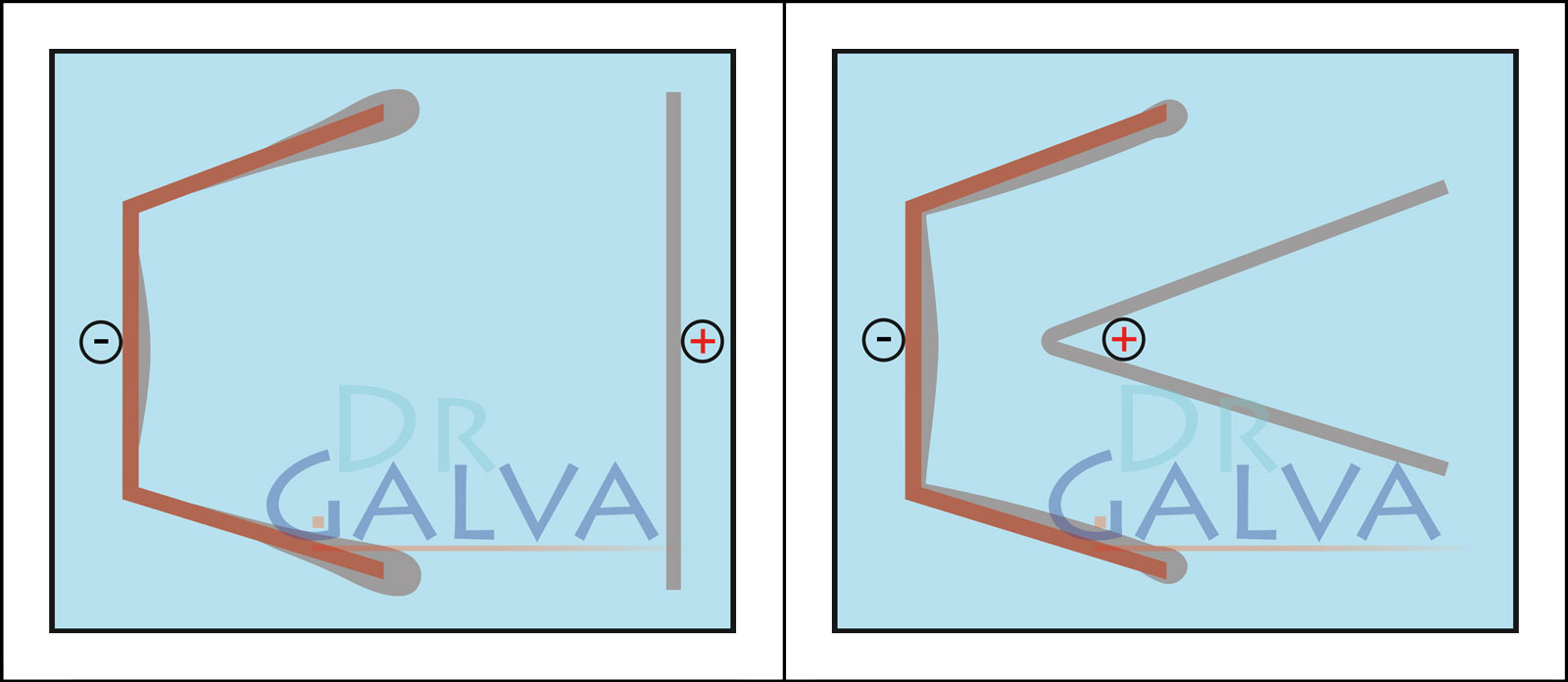
Dies ist die komplizierteste Form, das Metall scheidet sich fast nur im zur Anode zugewandten Bereich ab. Mit einer an die Form angepasster Anode findet noch eine gute Abscheidung im Innenbereich statt, auch die Ecken werden beschichtet. Allerdings ist dies recht aufwendig. - Warum ist der Metallgehalt eher unwichtig?
-
Der Metallionen-Gehalt (z. B. Cu²⁺, Ni²⁺, Zn²⁺) ist zweifellos eine wichtige Stellgröße eines galvanischen Elektrolyten – aber er ist eben nur eine von vielen, und in der Praxis fast nie der limitierende Faktor für Schichtqualität, Wirtschaftlichkeit oder Prozessstabilität. Die wesentlichen Gründe:
Warum er nicht „das Wichtigste“ ist Was stattdessen (mindestens) genauso zählt 1 . Begrenzter Einfluss jenseits eines Mindestwerts
Schon bei moderaten Konzentrationen ist die Ionenversorgung an der Kathode gesättigt. Höhere Metallwerte bringen nur geringen Stromdichte-Zuwachs, erhöhen aber Dichte, Viskosität und Schlamm-Bildung.Stromdichte & Stromverteilung
Über 90 % aller Schichtfehler (Burning, Flecken, Poren) hängen an lokaler Stromdichte – gesteuert durch Geometrie, Abstand, Rühren und Hilfsanoden, nicht durch den Metallgehalt.2 . Kristallstruktur wird von Additiven gesteuert
Glanz, Korngröße, innere Spannungen und Duktilität resultieren aus ppm-Bereichen organischer Carrier, Brightener, Leveller … völlig unabhängig davon, ob 20 g L⁻¹ oder 30 g L⁻¹ Ni²⁺ im Bad sind.Additivchemie & Abbauprodukte
Das Verhältnis von Carrier/Brightener verändert das Depot stärker als ±20 % Ni²⁺. Analytiklisten führen meist > 10 organische Parameter, aber nur einen Metallparameter.3 . Leitfähigkeit kommt eher von der Salzmatrix
Die ohmschen Verluste werden überwiegend durch Sulfat-, Chlorid- oder Borfluorid-Ionen bestimmt. Ein Silberbad enthält nur 2–3 g L⁻¹ Ag⁺, erreicht aber dank 150 g L⁻¹ KCN hohe Leitfähigkeit.Leitfähigkeits-Ionen & pH
pH regelt Wasserstoffabscheidung, Glanz und Spannungen; Puffersysteme (Borsäure, Citrat) stabilisieren Elektrolyt und Schicht.4 . Thermodynamik vs. Kinetik
Der Metallgehalt ändert kaum ΔG; die Abscheide-Kinetik wird von Temperatur, Rührgeschwindigkeit und Komplexierung (EDTA, Tartrat …) dominiert.Temperatur & Hydrodynamik
Eine Schwankung von ±5 K hat oft mehr Einfluss auf Schichtdicke-Verteilung als ±20 % beim Metall.5 . Badleben & Kostentreiber
Bei Cu- und Ni-Bädern liegen die Metallionen-Kosten < 20 % der Gesamtkosten pro m² Schicht; Additiv-Nachdosierung, Energie, Reinigung, Abwasser & Analytik sind höher.Verunreinigungs-Management
Spuren-Cu in Ni-Bädern oder Saccharinat-Abbau können ein Bad ruinieren, obwohl der Metallgehalt „ideal“ ist.6 . Metallgehalt definiert nicht die „Reichweite“
In erneuerbaren Elektrolyten ersetzt die Anodenauflösung das abgeschiedene Metall kontinuierlich. Die Reichweite eines Bades wird daher von Additiv-Abbau, Schmutzeintrag und Volumenverlust begrenzt – nicht vom Start-Metallgehalt.Anodenmaterial & Lösungsmechanik
Anodenreinheit, Chloridgehalt (bei Cu-OP-Bädern) und korrektes Stromdichte-Fenster bestimmen, wie effizient sich Cu, Ni, Zn etc. nachlösen. Ein gut geführtes Bad hält seinen Metallwert über Monate konstant, während die organischen Additive regelmäßig ergänzt werden müssen.Fazit: Der Metallionen-Gehalt bildet nur das Fundament des galvanischen Prozesses. Für Schichtqualität, Stabilität und Wirtschaftlichkeit sind Stromdichte-Management, Additive, Hydrodynamik, Temperaturführung, Anodenauflösung und Verunreinigungen wesentlich ausschlaggebender.
- Lösliche Anoden - Vorteile, Praxis, Grenzen
-
Lösliche Anoden bestehen aus dem zu abscheidenden Metall und lösen sich unter Strom auf. Dadurch füllen sie die Metallionen im Elektrolyten proportional zum Stromfluss auf – die Badzusammensetzung bleibt stabiler, ohne ständig Metallsalze nachzudosieren.
Vorteile löslicher Anoden
- Selbstnachspeisung der Metallionen: Anodenauflösung ≈ Metallabscheidung → geringerer Aufwand für Metallsalz-Nachdosierung.
- Kein Anionen-„Aufsalzen“: Statt mit jedem Nachsalzen Sulfat/Chlorid einzutragen, kommt nur Metall ins Bad → geringere Leitfähigkeits- und Volumenänderungen, weniger Korrekturen.
- Stabilere pH-/Redoxbedingungen: Oxidation läuft über Metallauflösung, nicht über Wasser/Chlorid → weniger O₂/Cl₂-Entwicklung, geringere Additiv-Oxidation.
- Niedrigere Zellspannung, bessere Energieeffizienz: Metallauflösung erfordert meist geringere Anodenpotenziale als Sauerstoffentwicklung.
- Konstantere Schichtqualität: Gleichmäßigere Metallaktivität fördert gleichmäßigen Glanz, Kornfeinheit und Abscheiderate.
- Praxisfreundlich: Weniger Chemiehandling, seltener Stillstand durch größere Nachansätze.
Typische Praxis
- Nickel: Schwefel-aktivierte Ni-Anoden / Ni-Pellets im Ti-Korb + etwas Chlorid zur Passivierungsvermeidung.
- Kupfer (sauer): P-haltige (phosphorierte) Cu-Anoden + Anodensäcke zur Schlammrückhaltung.
- Zinn, Zink u. a.: Weit verbreitet mit löslichen Anoden.
Grenzen / Nachteile
- Anodenschlamm & Passivierung → Anodensäcke, Filtration, passende Anodenstromdichte nötig.
- Metallische Verunreinigungen können mit aufgelöst werden (Anodenqualität wichtig).
-
Nicht immer geeignet:
- Chrom(VI)-Bäder arbeiten mit unlöslichen Anoden (kein Metallionenzuwachs, andere Elektrochemie gewünscht).
- Chrom(III)-Bäder: Verwendung von Chrom-Metallanoden kann Cr(VI) erzeugen und den Elektrolyten schädigen; nachteilig ist, dass Cr(III) durch die Abscheidung abgereichert wird, was die Reichweite begrenzt.
- Warum Glanzauffrischer, obwohl durch die Anoden angereichert wird?
-
Kurz gesagt: Anoden liefern (fast nur) Metallionen – Glanz kommt von organischen Zusätzen. Diese Zusätze entstehen nicht an der Anode und werden im Betrieb ständig verbraucht oder abgebaut. Darum braucht der Badbetrieb regelmäßig Glanzauffrischer.
Warum die Anodenanreicherung nicht reicht
- Anoden lösen Metall auf (z. B. Ni²⁺, Cu²⁺) und halten so die Metallkonzentration konstant. Organische Additive (Carrier/Suppressor, Brightener/Accelerator, Leveler) kommen von außen – nicht aus der Anode.
- Verbrauch an der Kathode: Additive adsorbieren an der Oberfläche; einige werden mitabgeschieden oder elektrochemisch reduziert/zerlegt. Das ist stromstärken- bzw. Ah-abhängig.
- Abbau an der Anode: Ein Teil der organischen Komponenten wird dort oxidiert (besonders in chloridhaltigen Bädern oder bei hoher Anodenpolarisation).
- Nebenverluste: Drag-out an Werkstücken/Warenträgern, Adsorption im Filter/Anodensack, thermischer/chemischer Abbau sowie Abreinigung (z. B. Aktivkohlebehandlung) entfernen Additive aus dem Bad.
Rolle des Glanzauffrischers
- Er enthält meist die kurzlebigen, stark wirksamen Bestandteile (häufig die „Accelerator/Glanz“-Fraktion), die am schnellsten verbraucht werden.
- Ohne Nachdosierung verliert der Niederschlag Glanz, Egalisierung und Feinkorn; es drohen Mattstellen, erhöhte Spannungen oder Rauheit.
Fazit
Die Anode ersetzt das Metall, der Glanzauffrischer ersetzt die funktionalen organischen Additive – beides ist nötig für konstante, glänzende Schichten.
Hinweis zur Badlebensdauer
Während theoretisch bei regenerierbaren Elektrolyten die Reichweite durch die Auflösung der Anoden unbegrenzt ist, werden andere Zusätze verbraucht. Um den teuren Elektrolyten weiter nutzen zu können, ergänzt man diese Zusätze. Dennoch gilt: Ohne spezielle Reinigungsverfahren hält auch so der Elektrolyt nicht unbegrenzt – mit dieser Additivpflege lässt sich seine Reichweite jedoch um ein Vielfaches steigern.
- Wie baue ich eine Galvanikzelle zum Abscheiden von Metallen?
-
Eine Galvanikzelle zum Abscheiden von Metallen, auch als elektrolytische Zelle oder Galvanisierungszelle bezeichnet, ist eine Vorrichtung, die verwendet wird, um eine Metallschicht auf einem anderen Metall durch einen elektrochemischen Prozess abzuscheiden. Hier ist eine Schritt-für-Schritt-Anleitung zum Aufbau einer solchen Zelle:
Materialien:
- Stromquelle: Eine regelbare Gleichspannungsquelle.
- Anode: Zum Beispiel eine Kupferanode, wenn Kupfer abgeschieden werden soll, bei einigen Lösungen muss auch eine andere Anode verwendet werden - beachte die Hinweise zum Elektrolyt.
- Kathode (Werkstück): Das Metallstück, auf dem das andere Metall abgeschieden werden soll (z.B. ein Schmuckstück).
- Elektrolytlösung: Eine Lösung, die Metallionen des abzuschiedenden Metalls enthält (z.B. Kupferelektrolyt für die Kupferabscheidung).
- Behälter: Um die Elektrolytlösung zu halten.
- Leitungsdrähte und Krokodilklemmen: Um die Elektroden mit der Stromquelle zu verbinden.
Aufbau:
-
Vorbereitung der Elektrolytlösung:
- Fülle den Behälter mit der Elektrolytlösung. Für die Abscheidung von Kupfer kannst du zum Beispiel einen Kupferelektrolyt verwenden.
- Fülle den Behälter mit der Elektrolytlösung. Für die Abscheidung von Kupfer kannst du zum Beispiel einen Kupferelektrolyt verwenden.
-
Einsetzen der Elektroden:
-
Anode: Setze die Anoden (z.B. die Kupferplatte) in die Lösung ein. Diese Elektroden werden das Metall liefern, das abgeschieden werden soll. Es sollten 2 gegenüberliegende Anoden verwendet werden, um eine gleichmäßigere Abscheidung zu erreichen. Beachte hierzu die Grafiken. (Sollte es nicht möglich sein, eine derartige Anodenanordnung zu erreichen, kann eine gleichmäßige Beschichtung des Werkstücks durch kontinuierliches Drehen erreicht werden.)
Beachte hierzu auch den Bereich "Die Streuung in der Galvanik"
-
Kathode: Setze die Kathode (z.B. das Schmuckstück) ebenfalls in die Lösung ein. Dies ist das Werkstück, auf dem das Metall abgeschieden wird.
-
Anode: Setze die Anoden (z.B. die Kupferplatte) in die Lösung ein. Diese Elektroden werden das Metall liefern, das abgeschieden werden soll. Es sollten 2 gegenüberliegende Anoden verwendet werden, um eine gleichmäßigere Abscheidung zu erreichen. Beachte hierzu die Grafiken. (Sollte es nicht möglich sein, eine derartige Anodenanordnung zu erreichen, kann eine gleichmäßige Beschichtung des Werkstücks durch kontinuierliches Drehen erreicht werden.)
-
Verbindung mit der Stromquelle:
- Verbinde die Anode (Kupferplatte) mit dem positiven Pol der Stromquelle.
- Verbinde die Kathode (Werkstück) mit dem negativen Pol der Stromquelle. Dadurch wird die Kathode negativ geladen, was zur Abscheidung des Metalls auf ihr führt.
-
Stromfluss einschalten:
- Schalte die Stromquelle ein. Die Metallionen in der Lösung (z.B. Cu²⁺-Ionen) werden von der Kathode angezogen, da sie negativ geladen ist. Die Ionen werden zu neutralen Metallatomen reduziert und lagern sich auf der Oberfläche der Kathode ab.
Funktionsweise:
-
Anode (Kupferplatte): Die Anode löst sich durch den Stromfluss teilweise auf, wobei Kupferionen (Cu²⁺) in die Lösung freigesetzt werden, dadurch bleibt die Konzentration der Kupferionen in der Elektrolytlösung konstant:
Cu → Cu²⁺ + 2e⁻
-
Kathode (Werkstück): An der Kathode werden die Kupferionen (Cu²⁺) aus der Lösung durch die Elektronen reduziert und als metallisches Kupfer auf dem Werkstück abgeschieden:
Cu²⁺ + 2e⁻ → Cu
Wichtige Hinweise:
- Stromstärke und Zeit: Die Stromstärke und die Dauer des Prozesses bestimmen die Dicke der abgeschiedenen Metallschicht. Höhere Stromstärken und längere Zeiten führen zu dickeren Schichten.
- Temperatur: Die Temperatur der Elektrolytlösung kann die Abscheidungsrate beeinflussen. Höhere Temperaturen können den Prozess beschleunigen, aber auch die Qualität der Schicht beeinflussen.
- Reinheit der Elektrolytlösung: Verunreinigungen in der Lösung können die Qualität der abgeschiedenen Metallschicht beeinträchtigen.
Ergebnis:
Durch diesen Aufbau wird eine gleichmäßige Metallschicht auf dem Werkstück abgeschieden. Dies ist das grundlegende Prinzip der Galvanisierung, das in vielen industriellen Prozessen verwendet wird, um Metalle zu beschichten und Oberflächen zu schützen oder zu veredeln.
Allgemeiner Aufbau:
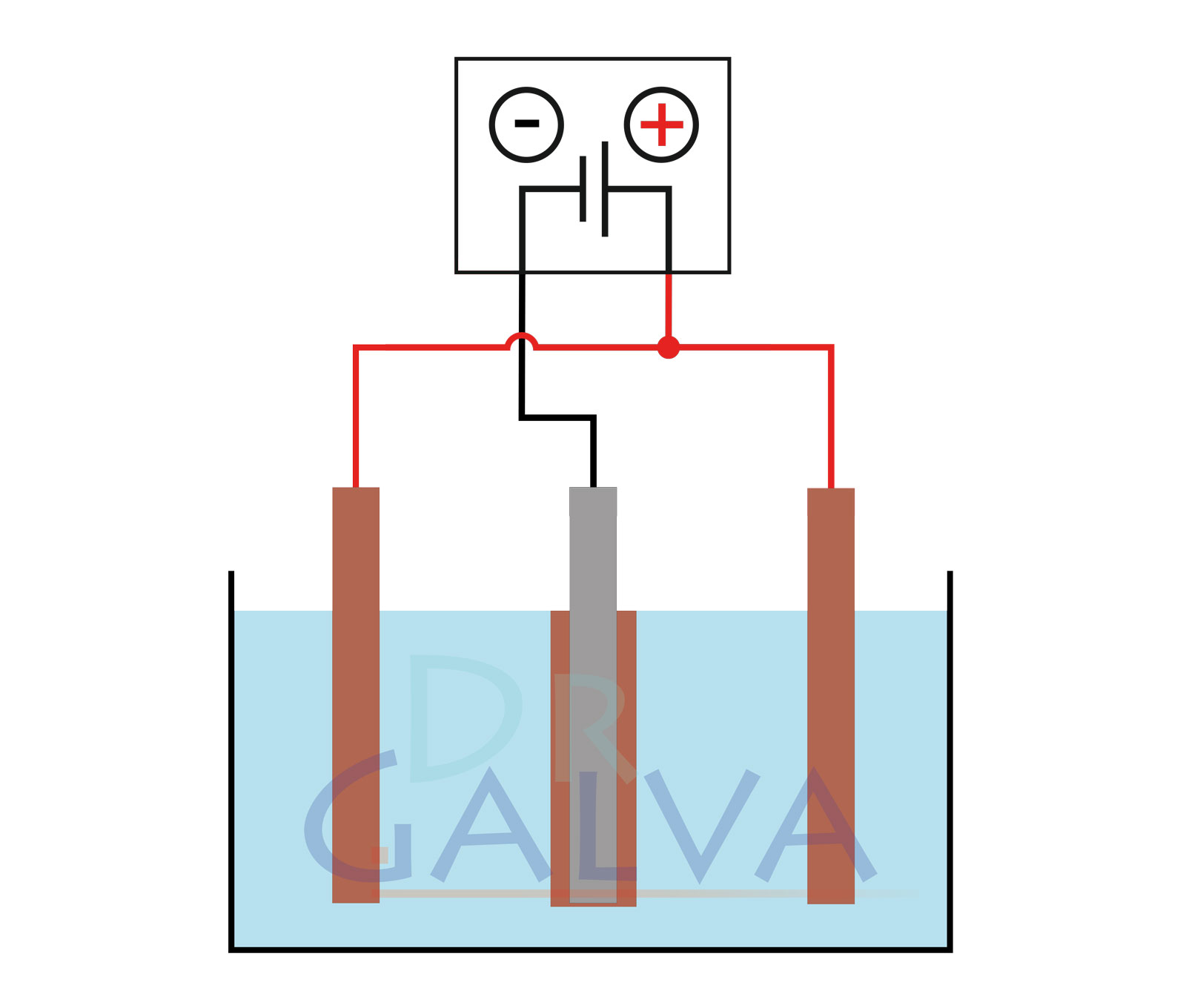
Vergleich der Abscheidung:
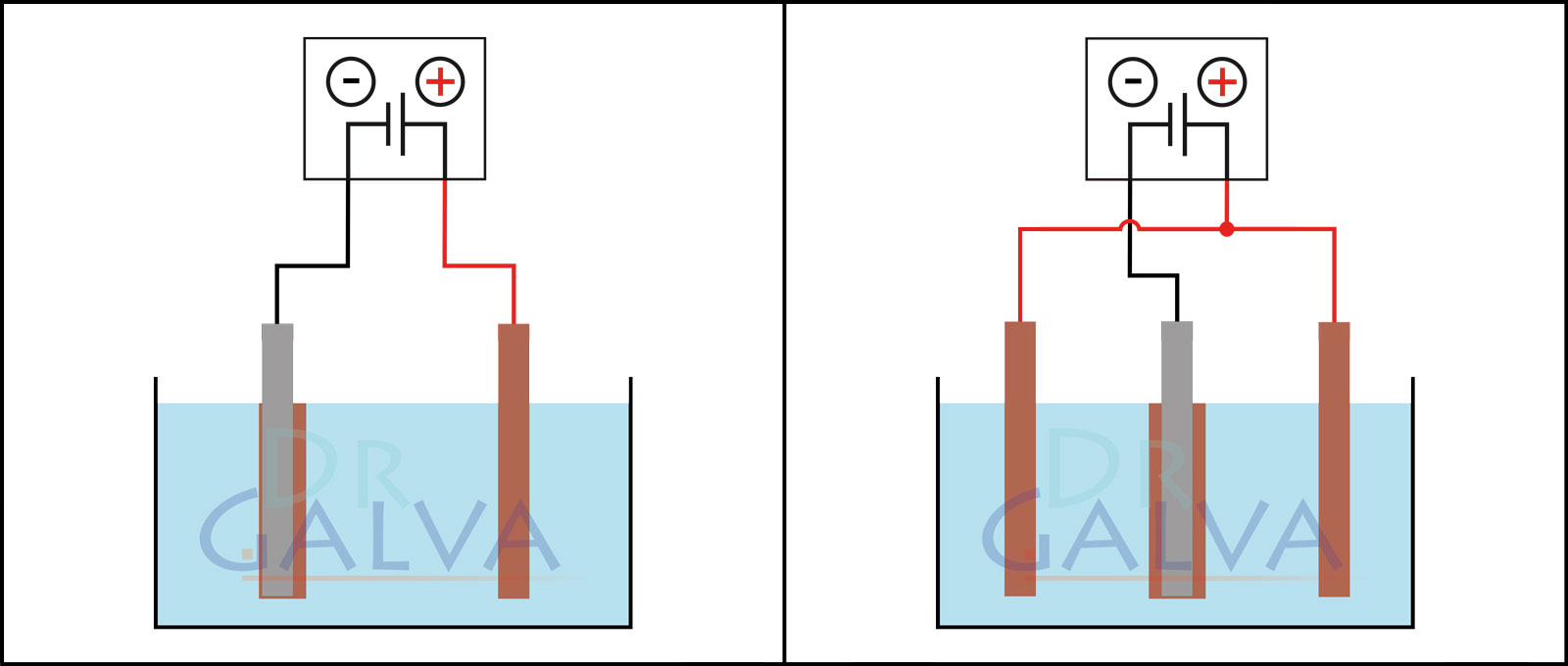
Die Anode und das Werkstück nehmen eine sich gegenüberliegende Position ein. Es wird an der Frontalseite des Werkstücks mehr Metall abgeschieden als auf der hinteren Seite. Das Werkstück sollte in regelmäßigen Abständen gedreht werden. Zwei Anoden und das Werkstück befinden sich in der Wanne. Zu beachten ist, dass beide Anoden mit dem gleichen Netzgerät verbunden sein sollten. Das Werkstück ist mittig, zwischen den beiden Anoden platziert. Hierdurch wird eine gleichmäßigere Abscheidung gewährleistet. - Richtiges Entfetten von zu beschichtenden Oberflächen
-
Das richtige Entfetten von zu beschichtenden Oberflächen ist ein entscheidender Schritt im Galvanikprozess. Eine gründliche Reinigung ist notwendig, um eine einwandfreie Haftung der Metallbeschichtung sicherzustellen und die Qualität der Endprodukte zu gewährleisten. Hier sind die wichtigsten Schritte und Methoden für das effektive Entfetten:
Warum ist Entfetten wichtig?
- Adhäsion: Fett- und Ölreste können die Haftung der galvanischen Beschichtung erheblich beeinträchtigen.
- Qualität der Beschichtung: Verunreinigungen führen zu ungleichmäßigen Beschichtungen, Blasenbildung und anderen Defekten.
- Korrosionsschutz: Saubere Oberflächen gewährleisten eine bessere Korrosionsbeständigkeit der beschichteten Materialien.
Methoden des Entfettens
1. Chemisches Entfetten
- Lösungsmittelreinigung: Verwendung von organischen Lösungsmitteln wie Aceton oder Isopropanol, die Fette und Öle effektiv lösen.
- Aceton zeichnet sich durch seine hervorragende Fettlöslichkeit und den niedrigen Siedepunkt aus. Es wird am Institut hauptsächlich zur Reinigung bzw. zum Entfetten von Arbeitsgeräten verwendet. Aceton löst gut Fingerabdrücke und andere leichte Fette, ist jedoch weniger wirksam gegen Maschinenöl. Tatsächlich kann Aceton bei ölverschmutzten Werkstücken kontraproduktiv sein, da es Schmutzpartikel durch Adhäsionskräfte dauerhaft auf der Oberfläche haften lassen kann.
- Isopropanol (Propan-2-ol) lässt sich in unterschiedlichen Disziplinen anwenden und ist besonders vielseitig. Es wird beispielsweise zur Reinigung von Bildschirmen oder zum Entfernen von lästigen Aufklebern verwendet, die sonst unangenehme Kleberänder hinterlassen. Isopropanol eignet sich besonders für hartnäckige Aufgaben, bei denen andere Mittel versagen, da es Rückstände vollständig entfernt. Isopropanol hinterlässt keine Spuren, da es rückstandsfrei verdunstet, und verhält sich zu den meisten Materialien chemisch neutral. Es kann mit destilliertem Wasser verdünnt werden und ist gut geeignet für die Entfernung von Ölen und Fetten sowie die Reinigung vieler Oberflächen.
- Alkalisches Entfetten: Einsatz von alkalischen Reinigern, die in wässriger Lösung Fette und Öle emulgieren und entfernen.
- Säurebäder: In einigen Fällen werden saure Reinigungsmittel verwendet, insbesondere wenn Metalloxide oder Rost entfernt werden müssen.
2. Mechanisches Entfetten
- Bürsten und Schleifen: Einsatz von Bürsten oder Schleifmitteln, um grobe Verunreinigungen zu entfernen.
- Strahlen: Verwendung von Strahlmitteln wie Glasperlen oder Sand, um die Oberfläche gründlich zu reinigen.
3. Elektrolytisches Entfetten
- Anodisches Entfetten: Die Werkstücke werden als Anode in eine alkalische Lösung gehängt und unter Strom gesetzt, wodurch Fette und Öle durch Gasentwicklung entfernt werden.
- Kathodisches Entfetten: Die Werkstücke werden als Kathode verwendet, was oft eine sanftere Reinigung ermöglicht.
Schritte zum Entfetten
1. Vorbereitung
- Entfernen von grobem Schmutz und sichtbaren Verunreinigungen durch Abspülen oder mechanische Reinigung.
2. Chemisches oder mechanisches Entfetten
- Anwendung der gewählten Entfettungsmethode gemäß den spezifischen Anforderungen des Materials und der Verunreinigung. Für ölverschmutzte Werkstücke sollten alternative Lösungsmittel oder Entfettungsmethoden gewählt werden, die effektiver als Aceton sind.
3. Spülen
- Gründliches Spülen der Teile mit destilliertem oder deionisiertem Wasser, um alle Rückstände des Entfetters zu entfernen.
4. Trocknen
- Sorgfältiges Trocknen der Oberfläche, um Wasserflecken oder erneute Verunreinigungen zu vermeiden.
Tipps für ein optimales Ergebnis
- Temperaturkontrolle: Viele Entfettungsprozesse sind bei erhöhten Temperaturen effektiver.
- Kontrollierte Umgebung: Arbeiten in einer sauberen Umgebung verhindert erneute Kontamination.
- Qualitätskontrolle: Regelmäßige Überprüfung der Oberflächenreinheit, beispielsweise durch Wassertropfentest oder Kontaktwinkelmessung.
Durch die Beachtung dieser Schritte und Methoden stellen Sie sicher, dass die zu beschichtenden Oberflächen optimal vorbereitet sind, was zu einer hochwertigen und langlebigen Galvanikbeschichtung führt.
- Wie verwendet man die galvanischen Elektrolyte?
-
Die Elektrolyte werden unverdünnt angewendet, da es sich um einsatzfertige Lösungen handelt. Die jeweiligen Parameter des Elektrolyts stehen auf der Flasche, sowie die benötigte Anode. Die Spannungswerte können abweichen, da in den Lösungen das Ohmsche Gesetz gilt. Der Widerstand ist hier ausschlaggebend und je nach Abstand kann sich der Stromfluss erhöhen oder verringern. Noch genauer wird es, wenn man über die Stromdichte arbeitet.
Auch werden die Elektrolyte durch das Ausflösen der Metallanode angereichert, was die Reichweite erhöht (außer bei unlöslichen Anoden oder Fremdmetallanoden).
Auch ist zu bedenken, dass der Strom den kürzesten Weg nimmt.
- Wie viel kann man mit einem galvanischen Elektrolyt beschichten?
-
Die Menge an Material, die mit einem galvanischen Elektrolyt abgeschieden werden kann, hängt von verschiedenen Faktoren ab:
Wichtige Einflussfaktoren
- Stromstärke und Beschichtungszeit: Nach dem Faradayschen Gesetz ist die abgeschiedene Metallmenge direkt proportional zur Ladungsmenge (Strom × Zeit).
- Elektrolytzusammensetzung: Der Metallionengehalt im Elektrolyt bestimmt, wie lange er nutzbar ist, bevor eine Nachdosierung oder Regeneration nötig wird.
- Effizienz des Prozesses: Abscheidungswirkungsgrade variieren je nach Metall und Elektrolyt (z. B. Kupfer und Nickel haben höhere Wirkungsgrade als Chrom).
- Schichtdicke: Je dicker die Schicht sein soll, desto mehr Material wird verbraucht.
Praxisbeispiel
Ein Liter Kupferelektrolyt mit 100 g/l Kupfer kann theoretisch etwa:
- 0,1 m² mit 100 µm Schichtdicke oder
- 1 m² mit 10 µm Schichtdicke beschichten.
Wichtiger Hinweis
Die tatsächlich beschichtbare Fläche ist oft deutlich größer, wenn die richtigen Anoden verwendet werden. Bei löslichen Anoden (z. B. Nickel- oder Kupferanoden) wird das abgeschiedene Metall kontinuierlich nachgeliefert, sodass sich der Elektrolyt während des Prozesses regeneriert und deutlich länger genutzt werden kann.
- Sind die Elektrolyte wiederverwendbar?
-
Die Elektrolyte sind mehrfach verwendbar. Achte darauf, dass keine Verunreinigungen eingebracht werden durch Verschmutzungen oder falsche Anoden. Auch kann es passieren, dass sich das Werkstück bei ungeeigneter Wahl im Elektrolyten löst (z.B. verzinktes Stahl in stark saurem Elektrolyten).
- Lassen sich die Anoden mehrmals verwenden?
-
Ja, Anoden in der Galvanik können mehrmals verwendet werden. Die Wiederverwendung von Anoden ist wirtschaftlich sinnvoll, solange sie effektiv Metallionen liefern können. Hier sind einige allgemeine Hinweise:
-
Material der Anode: Anoden bestehen oft aus demselben Material, das abgeschieden werden soll (z. B. Nickel, Kupfer, Zink). Diese Anoden werden während des Galvanikprozesses abgebaut, da sie Metallionen in das Bad abgeben, die sich dann auf dem Werkstück (Kathode) absetzen.
-
Verschleiß der Anode: Mit der Zeit lösen sich Anoden teilweise im Elektrolyten auf, da sie die Quelle der Metallionen für den Beschichtungsprozess sind. Die Abnutzungsrate hängt von der Stromdichte, der Dauer des Galvanisierens und der Art des Elektrolyten ab.
-
Pflege und Wartung: Anoden sollten regelmäßig überprüft und bei Bedarf gereinigt werden, um Oxidschichten oder Ablagerungen zu entfernen, die die Effizienz beeinträchtigen könnten. Eine ordnungsgemäße Wartung kann die Lebensdauer der Anoden verlängern.
-
Typ des Galvanikprozesses: Einige Prozesse erfordern eine häufigere Erneuerung der Anoden als andere. Zum Beispiel werden Anoden beim Vernickeln langsamer verbraucht als in Prozessen mit höheren Stromdichten oder spezifischen chemischen Anforderungen.
- Ersetzen der Anoden: Wenn Anoden zu stark abgenutzt sind oder ihre Leistung abnimmt, müssen sie ersetzt werden, um eine gleichmäßige und qualitativ hochwertige Beschichtung sicherzustellen.
Insgesamt können Anoden in der Galvanik also mehrmals verwendet werden, solange sie in gutem Zustand sind und effizient arbeiten. Regelmäßige Überprüfung und Pflege sind entscheidend, um die Lebensdauer der Anoden zu maximieren.
-
Material der Anode: Anoden bestehen oft aus demselben Material, das abgeschieden werden soll (z. B. Nickel, Kupfer, Zink). Diese Anoden werden während des Galvanikprozesses abgebaut, da sie Metallionen in das Bad abgeben, die sich dann auf dem Werkstück (Kathode) absetzen.
- Sind andere Metalle als Anoden möglich?
-
In der Galvanik ist es entscheidend, dass nur speziell für den jeweiligen Prozess geeignete Anoden verwendet werden. Andere Anodenmaterialien sind unzulässig, da sie sich im Elektrolyten auflösen und diesen dadurch verunreinigen können. Diese Verunreinigung führt zu einer minderwertigen Beschichtung und kann den gesamten Galvanisierungsprozess erheblich beeinträchtigen. Daher ist es wichtig, die vorgeschriebenen Anoden zu verwenden, um die Qualität und Reinheit der galvanischen Beschichtung sicherzustellen.
- Kann man auch kleine Sachen mit einem großen Netzteil beschichten?
-
Ja, man kann auch kleine Gegenstände mit einem großen Netzteil beschichten, aber es ist wichtig, die Stromstärke sorgfältig zu regulieren. Ein leistungsstarkes Netzteil kann mehr Strom liefern, als für kleine Objekte erforderlich ist, was zu einer Überbeschichtung, ungleichmäßigen Schichten oder sogar Schäden am Werkstück führen kann.
Es wird empfohlen, den Strom auf die erforderliche Stromdichte (Strom pro Fläche) für das jeweilige Material und die Lösung einzustellen, um eine kontrollierte und gleichmäßige Beschichtung zu erzielen. Ein gutes Netzteil sollte die Möglichkeit bieten, Spannung und Strom fein zu justieren, damit auch kleine Objekte sicher und präzise beschichtet werden können.
- Kann ich eine Batterie statt eines regelbaren Netzteils verwenden?
-
Während es theoretisch möglich ist, eine Batterie anstelle eines regelbaren Netzteils für die Galvanik zu verwenden, raten wir dringend davon ab. Der Grund dafür liegt in der fehlenden Möglichkeit, die Spannung und Stromstärke präzise zu regulieren, was für eine erfolgreiche Galvanisierung unerlässlich ist.
Gründe, warum eine Batterie ungeeignet ist:
-
Keine Spannungskontrolle: Batterien liefern eine feste Spannung (z.B. 1,5V bei einer AA-Batterie oder 12V bei einer Autobatterie). Da bei der Galvanik die Spannung oft angepasst werden muss, um die Qualität der Beschichtung zu steuern, führt die feste Spannung einer Batterie häufig zu suboptimalen Ergebnissen. Dies kann zu ungleichmäßigen Schichten, unkontrollierter Gasentwicklung (wie Blasenbildung) und anderen unerwünschten Effekten führen.
-
Unkontrollierte Stromstärke: Die Stromstärke hängt von der Spannung der Batterie und dem Widerstand des elektrolytischen Bades ab. Ohne die Möglichkeit, den Strom präzise zu regulieren, kann es zu einem zu hohen Stromfluss kommen, der die Beschichtung beschädigen kann, oder zu einem zu niedrigen, der den Prozess ineffizient macht.
-
Sinkende Leistung: Im Laufe der Nutzung nimmt die Leistung der Batterie ab, was zu einer sinkenden Spannung führt. Dies beeinflusst direkt die Qualität und Gleichmäßigkeit der Beschichtung und kann den Prozess unvorhersehbar machen.
-
Gefahr von Fehlbeschichtungen: Durch die fehlende Regelbarkeit ist das Risiko von Fehlbeschichtungen oder sogar Beschädigungen des Werkstücks deutlich erhöht. Dies kann zu unnötigem Materialverlust und zusätzlichen Kosten führen.
Fazit:
Für qualitativ hochwertige und konsistente Galvanisierungsergebnisse ist es entscheidend, Spannung und Strom präzise steuern zu können. Eine Batterie, die keine Regelmöglichkeiten bietet, kann diese Anforderungen nicht erfüllen und führt häufig zu unbefriedigenden Ergebnissen. Daher empfehlen wir die Verwendung eines regelbaren Netzteils, das speziell für die Anforderungen der Galvanik entwickelt wurde, um optimale Ergebnisse zu erzielen
-
- Kann man verschiedene Elektrolyte mischen?
-
Elektrolyte sollten nicht gemischt werden, da sie chemisch und elektrochemisch nicht kompatibel sind. Besonders alkalische und saure Elektrolyte dürfen nicht kombiniert werden – ihre unterschiedlichen pH-Werte führen zu unerwünschten Reaktionen, wie der Ausfällung von Metallen oder anderen Substanzen. Dadurch wird der Elektrolyt unbrauchbar und die Beschichtung fehlerhaft oder ungleichmäßig.
Auch das Mischen verschiedener Metall-Elektrolyte funktioniert nicht. Beispielsweise lassen sich Kupfer- und Zinkelektrolyt nicht einfach kombinieren, um Messing abzuscheiden. Die Metallionen verhalten sich in der Lösung unterschiedlich, sodass keine gleichmäßige Legierung entsteht.
Zudem sind die enthaltenen Zusätze exakt auf den jeweiligen Elektrolyten und dessen pH-Wert abgestimmt. Durch eine Mischung verlieren sie ihre Wirkung, und die gewünschten Eigenschaften des Elektrolyten gehen verloren.
- Woran erkennt man, dass der Elektrolyt verbraucht ist?
-
Eine Erschöpfung zeigt sich oft durch verlangsamte Abscheidung oder veränderte Farbe der abgeschiedenen Metallschicht. Ebenso kann die ursprüngliche Färbung des Elektrolyten verblassen oder der Glanz der Beschichtung nachlassen.
Um den Metallgehalt konstant zu halten, sollte stets eine geeignete Metallanode verwendet werden. Diese löst sich während des Prozesses langsam auf und reichert den Elektrolyten mit den benötigten Metallionen an. Dennoch kommt es im Laufe der Zeit zu Verunreinigungen (Fremdionen, organische Rückstände, Polymerisation), und Glanzbildner (falls vorhanden) werden verbraucht.
Für diesen Fall bieten wir Glanzauffrischer an, die fehlende Glanzbildner und weitere Additive gezielt ergänzen.
Bei Elektrolyten mit unlöslichen Anoden (z. B. Gold) findet keine automatische Metallnachführung statt.
Auch Chromelektrolyt lässt sich nur sehr aufwendig regenerieren. Da Chrom in der Regel nur als dünne Deckschicht auf Nickel abgeschieden wird, spielt dies jedoch eine untergeordnete Rolle.
- Entsorgung der Lösungen
-
Die verbrauchten Lösungen können an einer Schadstoffsammelstelle abgegeben werden. Kleinstmengen können meist verdünnt mit dem Abwasser entsorgt werden.
Informiere dich aber unbedingt über deine regionalen Bedingungen.
- Wo finde ich das Sicherheitsdatenblatt?
-
Dies findest du auf der Artikelseite im Reiter "Dokumente", hier kannst du es direkt runterladen/öffnen.
- Lassen sich Kunststoffe galvanisch beschichten?
-
Ja, Kunststoffteile lassen sich galvanisch beschichten. Ursprünglich wurde die Oberfläche der Kunststoffe hierfür mit Chromschwefelsäure geätzt und anschließend mit Palladium aktiviert. Da diese Substanzen jedoch sehr giftig und umweltschädlich sind, kommt zunehmend ein umweltfreundlicheres Verfahren zum Einsatz: ein leitfähiger Lack. Der Leitlack macht den Kunststoff leitfähig und verzichtet dabei auf umweltschädliche Chemikalien. Dieses Verfahren ist daher deutlich sicherer und nachhaltiger.
Ablauf des galvanischen Beschichtens von Kunststoffen mit Leitlack:
- Oberflächenvorbehandlung: Der Kunststoff wird gründlich gereinigt, um Fett, Staub und andere Verunreinigungen zu entfernen, die die Haftung beeinträchtigen könnten.
- Auftragen des Leitlacks: Ein spezieller Leitlack, der Metallpartikel (z. B. Kupfer- oder Silberpartikel) enthält, wird gleichmäßig auf die Kunststoffoberfläche aufgetragen. Dieser Lack sorgt dafür, dass die Oberfläche elektrisch leitfähig wird und als Basis für den galvanischen Prozess dient.
- Erstbeschichtung (z. B. saures Kupfer): Die mit dem Leitlack behandelte Oberfläche wird galvanisch mit einer dünnen Schicht aus saurem Kupfer beschichtet, um eine stabile, durchgehende Leitfähigkeit zu gewährleisten.
- Galvanische Beschichtung: Nun kann der Kunststoff mit der gewünschten Metallschicht (z. B. Nickel, gefolgt von Chrom oder Gold) beschichtet werden. Schichtdicke und Metallauswahl richten sich nach den spezifischen optischen und funktionalen Anforderungen.
Vorteile des Verfahrens mit Leitlack:
- Umweltfreundlicher: Verzicht auf Chromschwefelsäure und Palladium, wodurch die Umweltbelastung und Gesundheitsrisiken erheblich reduziert werden.
- Flexibel anwendbar: Der Leitlack lässt sich auf viele verschiedene Kunststoffarten auftragen und ermöglicht eine gleichmäßige Beschichtung.
- Effizient: Der direkte Übergang vom Leitlack zur galvanischen Beschichtung sorgt für einen schnellen, kosteneffizienten Prozess.
Anwendungsbereiche:
- Automobilindustrie: Verchromte Kunststoffteile wie Zierleisten und Embleme, hergestellt ohne umweltschädliche Chemikalien.
- Konsumgüter und Elektronik: Veredelung und Funktionalisierung von Kunststoffgehäusen und dekorativen Elementen.
Der Einsatz von Leitlacken als Alternative zu Chromschwefelsäure und Palladium ist eine nachhaltige, zukunftsweisende Lösung für viele Anwendungen in der Kunststoff-Galvanik.
- Edelstahl galvanisch beschichten
-
Edelstahl kann galvanisch beschichtet werden, erfordert jedoch eine spezielle Vorbehandlung. Die passive Oxidschicht auf Edelstahl erschwert die Haftung metallischer Überzüge. Der bewährte Weg zu einer erfolgreichen Beschichtung ist die Verwendung eines Nickel-Strike als Aktivierungsschicht.
Schritt-für-Schritt-Anleitung
1. Oberflächenreinigung
- Entfernen von Fett, Öl oder Verunreinigungen mit einem geeigneten Reiniger.
- Anschließendes gründliches Spülen mit deionisiertem Wasser.
2. Nickel-Strike als Haftvermittler
- Eine dünne Nickelschicht wird elektrochemisch abgeschieden.
- Diese sorgt für eine aktive Oberfläche und verhindert Ablösungen der Beschichtung.
- Nach dem Nickel-Strike sollte das Werkstück direkt in das nächste Galvanikbad überführt werden, ohne zu spülen.
3. Hauptbeschichtung aufbringen
Nach dem Nickel-Strike kann die gewünschte Metallschicht abgeschieden werden:
- Nickel für dekorative oder korrosionsbeständige Schichten.
- Kupfer als Zwischenschicht für weitere Beschichtungen.
- Chrom für glänzende und abriebfeste Oberflächen (es sollte eine dichte Nickelschicht vorliegen).
- Zink oder Zink-Nickel für Korrosionsschutz.
Warum ist Nickel-Strike notwendig?
- Edelstahl besitzt eine passive Chromoxidschicht, die eine direkte Metallabscheidung verhindert.
- Nickel-Strike entfernt diese Schicht und sorgt für eine haftfähige Oberfläche.
- Ohne Nickel-Strike hält die galvanische Beschichtung oft nicht dauerhaft auf Edelstahl.
- Wie beschichtet man Aluminium?
-
Sobald nicht beschichtetes Aluminium mit Sauerstoff in Kontakt kommt, setzt ein Oxidationsprozess ein. Dieser Prozess behindert jedoch die Beschichtung. Daher erfordern Werkstücke aus Aluminium immer eine Vorbehandlung mit einem Aluminiumaktivator. Dieser entfernt die Oxidschicht und erzeugt im gleichen Prozess eine Zinkschicht auf der Materialoberfläche. Auf diese Weise verhindert der Aktivator den Sauerstoffkontakt und schützt vor erneuter Oxidation. Um eine spätere Blasenbildung unter der Beschichtung zuverlässig zu verhindern, bieten wir unseren Kunden einen Aluminiumaktivator mit niedriger Viskosität.
Allerdings ist Zink nicht säurebeständig. Daher bringen Sie im nächsten Arbeitsschritt eine Schicht Kupfer alkalisch/basisch auf und anschließend eine Schicht aus saurem Kupferelektrolyt. So schaffen Sie eine stabile Grundlage für eventuell weitere Schichten.
Abhängig von der Aluminiumlegierung ist es erforderlich, die Oberfläche im ersten Schritt zu ätzen, bevor Sie die Zinkschicht mit dem Aluminiumaktivator aufbringen. Die aufgebrachte Zinkschicht wird nochmals geätzt und die Behandlung mit dem Aktivator ein zweites Mal wiederholt. Dies macht man, da die Zinkatschicht relativ rauh wird und sich so auch die Poren besser schließen. Das Zinkatverfahren ist leider als kompliziert anzusehen.
Um Aluminium zu Verchromen oder zu Vergolden wäre also folgende Reihenfolge erforderlich:
- Konditionierer zum Ätzen
- Aluminiumaktivator zum Erzeugen der Zinkatschicht
- Kupferelektrolyt alkalisch, um eine vor Säure schützende Kupferschicht zu erhalten
- Glanzkupferelektrolyt (sauer)
- Nickelelektrolyt (Free-Nickel), als Diffusionssperrschicht
- Chromelektrolyt oder Goldelektrolyt als abschließende Schicht
- Aluminiumaktivator für galvanische Beschichtungen
-
Wirkprinzip
Zinkat erzeugt auf Aluminium einen dünnen, haftfähigen Zink-Austauschfilm, der die sofortige Neubildung von Al-Oxid verhindert und die Oberfläche leitfähig/aktiv für nachfolgende elektrolytische Schichten (z. B. alkalisch Kupfer) macht.
Grundprinzip (Chemie)
In stark alkalischer Lösung (NaOH/KOH) wird die oberflächennahe Al-Matrix zu Aluminat gelöst; gleichzeitig scheidet sich aus komplex gebundenem Zink (z. B. Zn(OH)42−) elementares Zink auf der Oberfläche ab → Austauschschicht.
Standardprozesskette (galvanisch)
- Entfetten (alkalisch), gründlich spülen.
- Alkalisch beizen (kurz), spülen.
- Entoxidieren/Desmut (z. B. salpetersäurehaltig oder Konditionierer), spülen.
- Zinkat (typ. 30–90 s; kurz halten, sonst spröder Film).
- Double-Zincate bei schwierigen Legierungen: Zinkat chemisch abziehen/aktivieren → erneut zinkatieren. (Die erste Schicht ist hier oft nicht haftfest und lässt sich abwischen.)
- Kurzer Aktivierungs-Dip (mild sauer), ohne zu trocknen direkt weiter in die Galvanik.
-
Galvanischer Strike bei niedriger Stromdichte:
- Cyanid-Kupfer-Strike (klassisch, sehr zuverlässig; toxisch/umweltrelevant) oder
- Kupfer alkalisch
- Danach Hauptschichten: z. B. Glanzkupfer zum Aufbau, dekoratives Nickel/Chrom usw.
Legierungsabhängigkeiten
- Al-Si-Guss (hoch Si), Al-Mg, hochfeste Al-Legierungen: fast immer Double-Zincate; ggf. längerer Entoxid-Schritt.
- Frisch gegossene/gestrahlte Oberflächen: Poren und Siliziuminseln sorgfältig aktivieren; Beiz- und Entoxidzeiten anpassen.
Typische Fehlerbilder & Gegenmaßnahmen
- Abblättern/Blasen: zu dickes/überaltertes Zinkat, Oxide/Schmutz, lange Stillstands-/Trocknungszeiten → kürzere Zinkatzeiten, Bäder frisch halten, schneller Nass-in-Nass-Transfer (≤ 1–2 min).
- Dunkelgrau: Zinkat erschöpft, Aktivierung unzureichend → Zinkat erneuern, Aktivierung optimieren.
- Rauheit/Randangriffe: Beizchemie zu aggressiv/zu lang → Zeiten/Ansätze korrigieren.
Badführung (Zinkat)
- Stark alkalisch, enthält Zn-Komplexe; mit der Zeit steigt die Aluminat-Beladung → Aktivität fällt.
- Maßnahmen: Filtration, Teilerneuerung/Nachdosierung, kurze Kontaktzeiten, konstante Temperatur/Alkalität.
Sicherheit/Umwelt
Zinkat ist ätzend → PSA (Handschuhe, Schutzbrille, Schürze), Spritzer vermeiden. Spülen alkalisch/sauber führen; Zn/Al-haltige Abwässer vorschriftsgemäß behandeln. Cyanid-Strikes erfordern strikte Arbeits- und Abwasserschutzmaßnahmen.
- Wie kann ich 3D-Druck galvanisch beschichten?
-
Die galvanische Beschichtung von 3D-gedruckten Objekten ist ein mehrstufiger Prozess, der einige spezialisierte Ausrüstung und Materialien erfordert. Hier sind die grundlegenden Schritte zur galvanischen Beschichtung eines 3D-gedruckten Objekts:
1. Vorbereitung des 3D-gedruckten Objekts
- Reinigung: Reinigen Sie das Objekt gründlich, um jeglichen Staub, Öl oder andere Verunreinigungen zu entfernen. Dies kann mit Isopropylalkohol oder einem anderen geeigneten Reinigungsmittel erfolgen.
- Glätten: Falls erforderlich, glätten Sie die Oberfläche des 3D-gedruckten Objekts, um eine gleichmäßige Beschichtung zu gewährleisten. Dies kann durch Schleifen oder chemisches Glätten erreicht werden.
2. Leitfähige Schicht auftragen
- Sprühbare leitfähige Farbe: Tragen Sie eine leitfähige Farbe oder Tinte auf das Objekt auf. Diese Farbe enthält oft Kupfer, Silber oder Graphit, um die Oberfläche leitfähig zu machen.
- Leitfähige Beschichtungsmaterialien: Alternativ können Sie das Objekt in eine leitfähige Lösung tauchen oder es mit einer leitfähigen Beschichtung besprühen.
3. Vorbereitung für die Galvanisierung
- Anode und Kathode befestigen: Befestigen Sie das 3D-gedruckte Objekt als Kathode in Ihrem Galvanisierungsbad. Die Anode besteht normalerweise aus dem Metall, das Sie auf das Objekt aufbringen möchten (z.B. Kupfer, Nickel). Beachten Sie die Daten zur Lösung.
- Elektrolytische Lösung: Stellen Sie sicher, dass Sie die richtige elektrolytische Lösung für das Metall verwenden, das Sie auftragen möchten. Jede Metallbeschichtung erfordert eine spezifische Lösung.
4. Galvanischer Prozess
- Stromquelle: Verbinden Sie die Anode und die Kathode mit einer Gleichstromquelle. Der Stromfluss ermöglicht die Übertragung von Metallionen von der Anode auf das Objekt.
- Parameter einstellen: Stellen Sie die richtigen Parameter (Stromstärke / Spannung) ein, um eine gleichmäßige Beschichtung zu erzielen.
5. Nachbearbeitung
- Reinigung: Entfernen Sie das Objekt aus dem Galvanisierungsbad und spülen Sie es gründlich mit Wasser ab, um alle Rückstände der elektrolytischen Lösung zu entfernen.
- Polieren und Versiegeln: Polieren Sie die beschichtete Oberfläche, um den gewünschten Glanz zu erzielen, und versiegeln Sie sie ggf. mit einem Klarlack oder einer anderen Schutzbeschichtung.
Materialien und Ausrüstung
- Leitfähige Farbe
- Galvanisierungsbad und elektrolytische Lösung
- für den Elektrolyten geeignete Anode
- Gleichstromquelle
- Reinigungsmittel und Polierwerkzeuge
Sicherheitshinweise
- Schutzausrüstung: Tragen Sie geeignete Schutzausrüstung, einschließlich Handschuhe, Schutzbrille und Atemschutz, um sich zu schützen.
- Lüftung: Stellen Sie sicher, dass der Arbeitsbereich gut belüftet ist, um die Dämpfe der verwendeten Chemikalien zu minimieren.
Die galvanische Beschichtung kann die mechanischen und ästhetischen Eigenschaften von 3D-gedruckten Objekten erheblich verbessern. Wenn Sie diese Schritte sorgfältig befolgen, können Sie hochwertige metallbeschichtete 3D-gedruckte Teile herstellen.
- Wie lässt sich Chrom beschichten?
-
Eine verchromte Oberfläche bietet neuen Beschichtungen keine ausreichende Haftung. Daher muss die bestehende Chromschicht entfernt werden. Verwenden Sie für diesen Vorgang speziell dafür entwickelte Chromentferner. Diese Entferner-Lösungen sind in der Anwendung besonders sicher. So verhindern beispielsweise spezielle Zusätze das Entstehen des hochgiftigen sechswertigen Chroms.
In der Regel befindet sich unter der alten Chromschicht eine Nickelschicht. Die muss mit einem speziell dafür entwickelten Aktivator für die neue Beschichtung reaktiviert werden. Um die erneute Bildung einer Oxidschicht zu verhindern, wird das Werkstück unmittelbar nach der Reaktivierung der Nickelschicht neu beschichtet.
Alternativ existiert auch ein Gold-Strike der sich direkt auf Chrom auftragen lässt. Diese basieren darauf, dass im Prozess die Oxidschicht reduziert wird und gleichzeitig Gold abgeschieden wird.
- Warum keine Chromanode? Und warum ist eine Aluminiumanode zulässig?
-
Dreiwertige Chromelektrolyte: Auswahl der Anoden
Bei dreiwertigen Chromelektrolyten herrschen andere chemische und elektrochemische Bedingungen als in klassischen, sechswertigen Chrombädern. Deshalb müssen Anoden so ausgewählt werden, dass sie die Badzusammensetzung nicht stören und keine gesundheitsgefährdenden Substanzen erzeugen.
Warum keine Chromanode in dreiwertigen Chromelektrolyten?
-
Dissolutionsverhalten von Chrom
In dreiwertigen Chrombädern liegt das Chrom bereits in der Oxidationsstufe +III vor, die vergleichsweise stabil ist. Eine Chrom-Anode könnte jedoch zu unkontrollierter Oxidation zu Chrom(VI) führen:-
Chrom(VI) (sechswertiges Chrom) ist hochgiftig und krebserregend. Bereits geringe Mengen im Bad stellen daher ein gravierendes Gesundheits- und Umweltrisiko dar.
-
Chrom(VI) (sechswertiges Chrom) ist hochgiftig und krebserregend. Bereits geringe Mengen im Bad stellen daher ein gravierendes Gesundheits- und Umweltrisiko dar.
-
Badstabilität
Dreiwertige Chrombäder sind gezielt darauf ausgelegt, möglichst wenig bis gar kein Cr(VI) zu enthalten. Eine Chrom-Anode würde dieses Gleichgewicht stören, da bei der elektrochemischen Oxidation Cr(VI) entstehen kann. Dies beeinträchtigt die Abscheidequalität und birgt erhebliche Gefahren.
-
Praxis: Inerte oder spezielle Anoden
- Platin- oder Iridium-Anoden sind sehr gute inerte Anoden, da sie gegenüber dem Elektrolyten äußerst beständig sind und praktisch kein Material abgeben. Sie sind allerdings kostspielig.
- Graphit-Anoden werden ebenfalls häufig eingesetzt, geben jedoch mitunter feine Graphitpartikel an das Bad ab (Erosion/Abrieb). Diese können sich auf der Oberfläche des Werkstücks niederschlagen und zu dunklen Abscheidungen führen.
Warum ist eine Aluminiumanode zulässig?
-
Schützende Oxidschicht (Passivierung)
Aluminium bildet an seiner Oberfläche eine dichte Aluminiumoxidschicht (Al₂O₃). Diese Schicht passiviert das Metall und reduziert damit die Auflösung von Aluminiumionen ins Bad erheblich.
-
Geringe Störung der Badchemie
Bei den üblichen Spannungs- und pH-Werten in dreiwertigen Chromelektrolyten verhält sich Aluminium weitgehend passiv. So gelangen nur vergleichsweise geringe Mengen Al³⁺-Ionen in den Elektrolyten, wodurch Zusammensetzung und pH-Wert kaum beeinflusst werden.
-
Aluminium löst sich, scheidet sich aber nicht ab
Obwohl etwas Aluminium tatsächlich in Form von Al³⁺ ins Bad übergeht, schlägt es sich praktisch nicht als metallische Schicht aus wässriger Lösung nieder.- Aluminiumabscheidung aus Wasserlösungen ist thermodynamisch sehr schwierig, weil Wasser viel leichter reduziert wird (Wasserstoffbildung).
- Daher entsteht kein unerwünschter Aluminiumüberzug auf den Werkstücken.
-
Verfügbarkeit und Kosten
Aluminium ist kostengünstig, leicht zu bearbeiten und – sofern die Passivierung zuverlässig funktioniert – ein praktikabler Anodenwerkstoff für dreiwertige Chrombäder.
Fazit
- Eine Chromanode würde in dreiwertigen Chrombädern zur unerwünschten Bildung von Cr(VI) führen, das hochgradig gesundheitsgefährdend ist.
- Aluminiumanoden sind aufgrund ihrer schützenden Oxidschicht zulässig, da sie den Elektrolyten kaum verunreinigen und keine giftigen Nebenprodukte erzeugen.
- Platin- und Iridium-Anoden gelten als sehr beständige inerte Anoden, sind jedoch kostspielig.
- Graphit-Anoden sind zwar preisgünstig, können aber durch Abnutzung Graphitpartikel abgeben, was zu dunklen Abscheidungen führen kann.
-
Dissolutionsverhalten von Chrom
- Galvanisches Verchromen – DIY deluxe: Schritt für Schritt zu perfekten Chromfinish!
-
Das Galvanisieren ist eine verlässliche Methode, um einzigartige Chrom-Oberflächen zu erzielen. Mit dieser DIY-Anleitung bieten wir eine einfache Schritt-für-Schritt-Anleitung, um Ihnen zu helfen, einen perfekten Chrom-Look zu erzielen . Profitieren Sie von unserer Erfahrung und erzielen Sie ein überzeugendes Ergebnis!
Verchromen lassen sich Metalle, wie: Stahl, Edelstahl, Bronze, Eisen, Messing, Kupfer und Zinkdruckguss. Die Chromoberfläche wird auf einer dicken Unterbeschichtung aus Nickel aufgebracht. Es handelt sich um eine langfristige und robuste Ausführung, die wenig anfällig für Verschleiß und Kratzer ist.
1. Einführung in Galvanisches Verchromen
Wenn Du Dich für das Galvanische Verchromen interessierst, dann bist Du hier genau richtig! Beim Galvanischen Verchromen handelt es sich um ein Verfahren, bei dem eine dünne Schicht aus Chrom auf ein Metall aufgetragen wird. Dieses Verfahren ist besonders beliebt, da es eine hohe Haltbarkeit und Beständigkeit aufweist. Zudem sieht das Chromfinish einfach klasse aus und verleiht jedem Werkstück das gewisse Etwas. Doch wie funktioniert das Galvanische Verchromen eigentlich? Zunächst wird das Werkstück in ein Bad mit Chromelektrolyt getaucht und mit einem Strom durchzogen. Dadurch wird das Chrom aus dem Elektrolyten auf das Werkstück übertragen und bildet eine Schicht aus Chrom. Um ein perfektes Ergebnis zu erzielen, solltest Du jedoch einige wichtige Tipps und Tricks beachten. So ist beispielsweise eine gründliche Reinigung des Werkstücks vor dem Verchromen unerlässlich. Auch die Wahl des richtigen Stromstärke und die Dauer des Verchromens spielen eine entscheidende Rolle. Mit diesen grundlegenden Informationen bist Du bestens gerüstet, um Dein Werkstück in ein glänzendes Highlight zu verwandeln.
2. Die wichtigsten Werkzeuge und Materialien
Um ein perfektes Chromfinish zu erzielen, benötigst Du die richtigen Werkzeuge und Materialien. Hier sind die wichtigsten Dinge, die Du brauchst: Zunächst benötigst Du eine Galvanik-Anlage, die aus einer Stromquelle, dem Chromelektrolyt und Anode besteht. Du benötigst auch eine geeignete Oberfläche, die Du verchromen möchtest. Diese sollte sauber und frei von Rost, Schmutz und Fett sein. Um dies zu erreichen, kannst Du Schleifpapier, Stahlwolle oder eine Drahtbürste verwenden. Zusätzlich benötigst Du noch eine Schutzbrille, Handschuhe und eine Atemmaske, um Dich vor den chemischen Dämpfen zu schützen. Mit diesen Werkzeugen und Materialien bist Du bereit, Dein eigenes Chromfinish zu kreieren.
3. Vorbereitung der Oberfläche für das Chromfinish
Bevor es ans eigentliche Verchromen geht, ist eine gründliche Vorbereitung der Oberfläche unerlässlich. Denn nur auf einer sauberen und glatten Oberfläche kann das Chromfinish perfekt haften und seine volle Wirkung entfalten. Zunächst solltest Du die zu verchromende Fläche gründlich reinigen und von Staub, Schmutz und Fett befreien. Hierfür eignet sich am besten ein spezieller Reiniger für Metall oder ein mildes Spülmittel. Anschließend solltest Du die Oberfläche mit feinem Schleifpapier oder einer Drahtbürste bearbeiten, um Unebenheiten und Rostansätze zu entfernen. Achte dabei darauf, nicht zu viel Material abzutragen und die Oberfläche nicht zu beschädigen. Abschließend solltest Du die Oberfläche noch einmal gründlich reinigen und trocknen lassen, bevor es ans eigentliche Verchromen geht. Mit einer sorgfältigen Vorbereitung der Oberfläche legst Du den Grundstein für ein perfektes Chromfinish und kannst Dich schon bald an einem glänzenden Ergebnis erfreuen.
4. Anwendung des galvanischen Verchromens
Wenn es um das Verchromen von Gegenständen geht, ist das galvanische Verfahren eine der besten Optionen. Es ist relativ einfach durchzuführen und liefert ein perfektes Ergebnis. Die Anwendung des galvanischen Verchromens erfordert jedoch einige wichtige Schritte, um sicherzustellen, dass das Chromfinish gleichmäßig und haltbar ist. Zunächst muss die Oberfläche des Gegenstands gründlich gereinigt werden, um sicherzustellen, dass keine Schmutzpartikel oder Fettreste vorhanden sind, die das Chromfinish beeinträchtigen könnten. Dann muss das Objekt in ein Bad mit einer speziellen Chromlösung eingetaucht werden, um eine Schicht aus Chrom auf der Oberfläche zu erzeugen. Es ist wichtig, dass das Objekt während des gesamten Prozesses ständig bewegt wird, um sicherzustellen, dass die Schicht gleichmäßig aufgetragen wird. Sobald die Chromschicht aufgetragen ist, muss das Objekt gründlich gespült und getrocknet werden, um das perfekte Chromfinish zu erzielen. Wenn du diese Schritte genau befolgst, wirst du in der Lage sein, jedes Objekt mit einer perfekten Chromschicht zu versehen und es so aussehen zu lassen, als ob es direkt aus einer professionellen Werkstatt stammt.
5. Nachbereitung der Oberfläche, um ein perfektes Finish zu erzielen
Nachdem Du den galvanischen Verchromungsprozess erfolgreich durchgeführt hast, ist es wichtig, die Oberfläche sorgfältig nachzubereiten, um ein perfektes Finish zu erzielen. Zunächst musst Du jegliche Verunreinigungen, wie Fingerabdrücke oder Staubpartikel, von der Oberfläche entfernen. Hierfür kannst Du ein weiches Tuch oder einen Mikrofasertuch verwenden. Anschließend solltest Du die Oberfläche mit einem speziellen Reinigungsmittel für Chrom polieren. Dieses entfernt nicht nur eventuelle Rückstände, sondern schützt auch die Oberfläche vor Korrosion und Oxidation. Zum Abschluss kannst Du die Oberfläche noch mit einem Wachs oder einer Versiegelung behandeln, um sie vor Kratzern und Beschädigungen zu schützen. Mit dieser Nachbereitung erzielst Du ein perfektes Chromfinish, das lange Zeit hält und Deinem Werkstück den letzten Schliff verleiht.
6. Tipps und Tricks für ein professionelles Ergebnis
Um ein professionelles Ergebnis beim galvanischen Verchromen zu erzielen, gibt es einige Tipps und Tricks, die du beachten solltest. Zunächst ist es wichtig, dass du alle Schritte genau befolgst und keine Abkürzungen nimmst. Auch das richtige Equipment ist entscheidend für ein perfektes Chromfinish. Achte darauf, hochwertige Materialien zu verwenden und investiere in eine gute Stromquelle. Eine gründliche Reinigung des zu verchromenden Objekts ist ebenfalls unerlässlich, um eine gleichmäßige Beschichtung zu gewährleisten. Zudem solltest du darauf achten, dass die Oberfläche des Objekts frei von Kratzern und Unebenheiten ist. Eine gute Vorbereitung und sorgfältiges Arbeiten sind also das A und O für ein professionelles Ergebnis beim galvanischen Verchromen.
7. Fazit: DIY deluxe – mit dem richtigen Know-how zum perfekten Chromfinish
Und voilà, das Ergebnis kann sich sehen lassen: Dein selbst verchromtes Werkstück erstrahlt in neuem Glanz und ist bereit für den Einsatz. Mit dem richtigen Know-how und ein wenig Geduld ist das galvanische Verchromen auch für Hobbybastler kein Problem. Wichtig ist, dass du dich an die Sicherheitsvorschriften hältst und die einzelnen Schritte sorgfältig ausführst. Mit dem richtigen Equipment und ein paar Tricks und Kniffen kannst du deinen DIY-Projekten ein edles und hochwertiges Finish verleihen. Also, worauf wartest du noch? Probiere es aus und verpasse deinen Werkstücken den perfekten Chrom-Look!
- Kupferelektrolyt alkalisch/basisch - Anwendungsbereiche
-
Sollen Eisen oder säureempfindliche Materialien wie Blei, Zink, Kupfer oder Stahl galvanisch verkupfert werden, bietet sich der Einsatz von "Kupferelektrolyt alkalisch" zur Vorbereitung an. So würde beispielsweise Zink ohne Vorbehandlung mit "Kupferelektrolyt alkalisch" in einem sauren Elektrolyten aufgelöst werden. Um dies zu verhindern, versieht das materialschonende alkalische Elektrolyt die säureempfindlichen Materialien mit einer ersten Kupferschicht und bereitet sie für die abschließende Beschichtung mit "Glanzkupferelektrolyt sauer" vor.
Ein weiterer positiver Effekt ist die hervorragende Hafteigenschaft der Schicht, die durch „Kupferelektrolyt alkalisch“ entsteht sowie der verbesserte Korrosionsschutz. Der alkalische Kupferelektrolyt von Dr. Galva zeichnet sich durch eine besonders feinkörnige Abscheidung aus und ist duktil.
- Was unterscheidet einen alkalischen und sauren Kupferelektrolyten?
-
In der Galvanik gibt es zwei Haupttypen von Kupferelektrolyten: alkalische und saure. Sie unterscheiden sich in ihrer Zusammensetzung, ihrem pH-Wert und den Eigenschaften der abgeschiedenen Kupferschichten.
Unterschiede zwischen alkalischen und sauren Kupferelektrolyten:
pH-Wert:
- Alkalischer Kupferelektrolyt: Hat einen hohen pH-Wert (basisch), oft basierend auf Salzen wie Kupfercyanid oder Kupfersulfat, zur Stabilisierung sind Komplexbildner enthalten.
- Saurer Kupferelektrolyt: Hat einen niedrigen pH-Wert (sauer) und basiert in der Regel auf Kupfersulfat und Schwefelsäure.
Abscheidungseigenschaften:
- Alkalischer Kupferelektrolyt: Eignet sich gut für das Beschichten von säureempfindlichen Materialien wie Zink oder Eisen. Er bietet eine gute Haftung auf diesen Materialien und erzeugt eine Schicht, die oft duktiler ist, das heißt, sie kann besser verformt werden, ohne zu brechen.
- Saurer Kupferelektrolyt: Eignet sich für glatte, dekorative Schichten mit einer glänzenden Oberfläche. Er wird oft für großflächige, einfache Metallteile verwendet und bietet eine schnellere Abscheidung und eine feinere Kristallstruktur.
Verwendung und Anwendungsbereich:
- Alkalischer Kupferelektrolyt: Wird häufig für komplex geformte Werkstücke und für eine gleichmäßige Abscheidung auf verschiedenen Substraten genutzt, insbesondere wenn gute Haftung und Duktilität wichtig sind. Er wird oft in der Elektronik, bei gedruckten Schaltungen und für Verkupferungen von Eisen verwendet.
- Saurer Kupferelektrolyt: Ist ideal für Anwendungen, bei denen eine glänzende, dekorative Oberfläche benötigt wird, und wird häufig für dekorative Beschichtungen auf Metallen verwendet, z.B. in der Schmuckindustrie oder für verchromte Oberflächen als Basis.
- Ich möchte Stahl verkupfern, muss ich sauer oder alkalisch wählen?
-
Für die Verkupferung von Stahlteilen sollte der alkalische Kupferelektrolyt gewählt werden. Bei Verwendung eines sauren Kupferelektrolyten kann es zu einer stromlosen Abscheidung von Kupfer auf dem Stahl kommen. Diese unkontrollierte chemische Reaktion führt zu einer grobkörnigen Kupferschicht mit schlechter Haftung, was die Qualität der Beschichtung beeinträchtigt.
Der alkalische Elektrolyt ermöglicht eine kontrollierte, elektrolytische Abscheidung des Kupfers, was zu einer gleichmäßigen und fest haftenden Schicht führt. Allerdings scheiden alkalische Elektrolyte leider nicht glänzend ab, sodass man danach oft zusätzlich sauer mit einem Glanzkupferelektrolyten verkupfert, um eine glänzende, dekorative Oberfläche zu erzielen. Daher ist es üblich, bei Stahlkomponenten zuerst den alkalischen Kupferelektrolyten für eine gute Haftung zu verwenden und anschließend einen sauren Kupferelektrolyten für das glänzende Finish.
- Warum ist ein saurer Kupferelektrolyt nur bedingt für Eisen geeignet?
-
Kupfer kann sich aufgrund des elektrochemischen Potentials stromlos auf Eisen abscheiden, da Kupfer edler ist als Eisen. Bei der stromlosen Abscheidung oxidiert das Eisen in der sauren Lösung, wodurch Kupferionen reduziert und auf der Eisenoberfläche abgeschieden werden.
Diese stromlose Abscheidung führt jedoch zu einer schlechten Haftung des Kupfers, da sich grobkörnige Kupferkristalle bilden, die die Verbindung zwischen Kupfer und Eisen schwächen.
Um diese Probleme zu mildern, kann man das Werkstück unter Spannung in die Lösung einbringen, wodurch die Kupferabscheidung elektrolytisch erfolgt. Die angelegte Spannung führt zu einer kontrollierten Abscheidung und verbessert dadurch die Haftung des Kupfers. Auf diese Weise lassen sich die Probleme der stromlosen Abscheidung weitgehend umgehen.
Um dieses Problem zu vermeiden, kann man eine dünne Schicht aus einem alkalischen Kupferelektrolyt aufbringen.
- Wie ist die Vorgehensweise beim alkalisch und danach glänzend Verkupfern?
-
1. Vorbereitung des Werkstücks
- Entfetten: Chemisch oder elektrolytisch, bis die Oberfläche völlig fettfrei ist.
- Beizen: Konditionierer, um Oxide zu entfernen.
- Abspülen: Gründlich mit VE-Wasser oder Leitungswasser spülen, damit keine Säurereste ins Kupferbad verschleppt werden.
2. Abscheidung im alkalischen Kupferbad
- Zweck: Dünne Haftschicht auf dem unedlen Grundmaterial.
- Bedingungen:
Schichtdicke nur 1-3 µm (nicht dicker, sonst steigt die Gefahr des Abblätterns). - Gleichmäßige Stromdichte einhalten, lieber etwas niedriger starten.
- Bedingungen:
- Abspülen: Direkt nach dem Prozess gründlich abspülen.
3. Abscheidung im sauren Glanzkupferbad
- Übergang: Werkstück nach dem Abspülen ins Glanzkupferbad überführen.
- Stromführung:
- Zunächst mit niedriger Stromdichte starten, damit die Schicht fein und haftfest anzieht.
- Danach langsam auf die normale Arbeitsstromdichte hochfahren.
- Schichtdicke: Beliebig aufbauen, je nach dekorativem oder funktionalem Bedarf.
Fehler:
Zu dicke alkalische Kupferschicht: Der Zweck der alkalischen Kupferschicht ist eigentlich nur, eine dünne, haftfähige Sperrschicht zu bilden. Eine zu dicke Schicht kann Spannungen erzeugen und später abplatzen.
Falsche Badparameter: Stromdichte oder Spannung zu hoch beim Start im Glanzkupfer - die noch nicht perfekt leitfähige Oberfläche bekommt „Brenner“ oder eine gestörte Kristallstruktur, die sich ablöst.
- Was macht Nickel-Strike?
-
Nickel-Strike ist eine sehr dünne, stark saure Haft-Zwischenschicht aus Nickel. Sie aktiviert passive bzw. schwierig zu beschichtende Oberflächen und sorgt so für deutlich bessere Haftung der folgenden Schichten.
Wofür braucht man’s?
- Edelstahl (V2A/V4A, hochlegierte Stähle): entfernt/passiviert die Chromoxid-Schicht und macht die Oberfläche „aktiv“.
- Bereits vernickelte Teile / Alt-Nickel: reaktiviert alte oder angelaufene Nickeloberflächen.
- Nach dem Entchromen: aktiviert das darunterliegende Nickel für die Weiterbeschichtung.
Nicht geeignet / besser: Alu → Aluminium-Aktivierer (Zinkat); Zink/Zamak → zuerst alkalisches Kupfer; normaler Baustahl → meist reicht Konditionierer.
Wie funktioniert’s?
- Stark saurer, chloridhaltiger Nickel-Elektrolyt wird kurz bei relativ hoher Stromdichte gefahren.
- Beizt Oxide an und erzeugt eine sehr dünne, raue Nickel-Keimschicht (typisch Zehntel-µm).
- Diese Keimschicht liefert hervorragende Haftung für Haupt-Nickel, ggf. Kupfer – und damit auch für Chrom (Chrom nur auf Nickel).
Praxis-Tipps
- Reihenfolge: gründlich entfetten → spülen → Nickel-Strike → direkt nass-in-nass ins Haupt-Nickel.
- Kurz halten: zu langes Striken kann Schicht spröde machen/Unterwanderung fördern.
- Badpflege: Lösung sauber/frisch halten; zu niedrige Stromdichte = unzureichende Aktivierung.
Merksatz: Chrom immer nur auf Nickel – Nickel-Strike macht schwierige Oberflächen überhaupt erst „nickelfähig“.
- Wie beschichtet man angelaufenes Nickel?
-
Angelaufenes Nickel war über längere Zeit dem Kontakt mit Sauerstoff ausgesetzt. Dadurch bilden sich Oxide, die Sie mit unserem Nickel-Strike entfernen können und zugleich eine tragfähige Nickelschicht aufbauen. Im Anschluss daran führen Sie die gewünschte Beschichtung durch.
Eine Vorbehandlung mit Nickel-Strike ist nicht erforderlich, wenn die Nickelschicht unmittelbar vor der weiterführenden Beschichtung aufgebracht wurde. Eine neu Nickelschicht sollte innerhalb einer Stunde weiterbeschichtet werden, da sich die Oxidschicht langsam aufbaut.
- Ist der Free-Nickel Nickelelektrolyt nickelfrei?
-
Nein, der Free-Nickel Nickelelektrolyt ist nicht nickelfrei. Der Name „Free-Nickel“ bezieht sich darauf, dass dieser Elektrolyt frei verkauft werden darf, da er die gesetzlichen Bestimmungen für den Verkauf an Privatpersonen erfüllt. Viele herkömmliche Nickelelektrolyte unterliegen in der EU strengen Beschränkungen und dürfen nicht über den Versandhandel verkauft werden.
Der Free-Nickel Nickelelektrolyt hingegen wurde speziell entwickelt, um diese Anforderungen zu erfüllen und kann daher ohne Einschränkungen online erworben werden. Bitte beachten Sie, dass es sich dennoch um einen Nickelelektrolyt handelt, der Nickel abscheidet und somit Nickel enthält.
- Wie man galvanisch vernickelt: Einfaches DIY-Tutorial
-
Galvanisches Vernickeln ist eine einfache und kostengünstige Methode, um Metallteile schnell und effizient zu schützen. In unserem DIY-Tutorial erfahren Sie alles, was Sie wissen müssen, um Ihre Metallteile selbst zu vernickeln. Lernen Sie, wie Sie Ihre Projekte schnell und effektiv schützen und verleihen können! Nichts ist besser als die Zufriedenheit, ein eigenes Projekt erfolgreich zu vervollständigen. Also, worauf warten Sie? Los geht's!
1. Warum galvanisch vernickeln?
Wenn du dich fragst, warum galvanisch vernickeln eine gute Option ist, gibt es einige Gründe. Zum einen bietet das Verfahren eine hohe Korrosionsbeständigkeit, was bedeutet, dass das vernickelte Objekt länger hält und weniger anfällig für Rost und ähnliche Schäden ist. Darüber hinaus verleiht das Verfahren dem Objekt eine glänzende und gleichmäßige Oberfläche, die nicht nur ästhetisch ansprechend ist, sondern auch eine bessere Leitfähigkeit bietet. Galvanisch vernickeln kann auch dazu beitragen, dass das Objekt widerstandsfähiger gegen Verschleiß und Abrieb wird, was besonders nützlich ist, wenn es regelmäßig beansprucht wird. Insgesamt bietet das galvanische Vernickeln eine Vielzahl von Vorteilen, die es zu einer attraktiven Option für diejenigen machen, die ihre Objekte schützen und verbessern möchten.
2. Was ist Galvanisierung und wie funktioniert es?
Galvanisierung ist ein Prozess, bei dem eine Metallschicht auf ein anderes Material aufgebracht wird. Es ist eine gängige Methode, um Metallteile zu schützen oder ihnen ein dekoratives Aussehen zu verleihen. Der Prozess der Galvanisierung erfolgt durch Elektrolyse, bei der ein elektrischer Strom durch eine Lösung geleitet wird, die das Metall enthält, das auf das zu beschichtende Material aufgebracht werden soll. Das zu beschichtende Material wird als Kathode bezeichnet, während das Metall, das aufgebracht werden soll, als Anode bezeichnet wird. Wenn der Strom durch die Lösung fließt, werden Metallionen von der Anode abgegeben und auf die Kathode abgeschieden, wodurch eine dauerhafte Metallschicht entsteht. Die Dicke der Schicht hängt von der Dauer des Prozesses ab. Galvanisierung kann für eine Vielzahl von Materialien wie Stahl, Kupfer, Messing und Aluminium verwendet werden. Es ist eine kostengünstige und einfache Methode, um Metallteile zu schützen oder ihnen ein dekoratives Aussehen zu verleihen.
3. Welche Werkzeuge braucht man für ein DIY-Projekt?
Wenn du ein DIY-Projekt durchführen möchtest, ist es wichtig, die richtigen Werkzeuge zur Hand zu haben. Für das galvanische Vernickeln benötigst du einige spezielle Werkzeuge, die dir helfen, das Projekt erfolgreich abzuschließen. Zunächst benötigst du eine Stromquelle wie eine Batterie oder ein Netzteil. Außerdem benötigst du einen Elektrolyten, der das Nickel auf das Metall aufträgt. Eine Nickelanode und ein Kathodenmaterial sind ebenfalls notwendig. Weiterhin benötigst du ein geeignetes Reinigungsmittel, um das Metall vor der Vernickelung zu reinigen. Ein Schleifpapier oder eine Drahtbürste können ebenfalls hilfreich sein, um das Metall vorzubereiten. Vergiss nicht, Schutzhandschuhe und Schutzbrille zu tragen, um dich vor Verletzungen zu schützen. Mit diesen Werkzeugen und ein wenig Übung kannst du dein DIY-Projekt erfolgreich galvanisch vernickeln.
4. Schritt-für-Schritt Anleitung zur galvanischen Vernickelung
Um galvanisch zu vernickeln, benötigst Du einige spezielle Materialien und Werkzeuge. Zunächst musst Du die zu vernickelnden Teile gründlich reinigen und entfetten, um sicherzustellen, dass die Nickelbeschichtung gut haftet. Dann musst Du eine Nickelbadlösung herstellen und diese in einem geeigneten Behälter platzieren. Als nächstes musst Du eine Stromquelle anschließen und die zu vernickelnden Teile als Kathode in die Lösung tauchen. Der Anodenstab sollte in die Lösung getaucht werden, aber nicht in Kontakt mit den zu vernickelnden Teilen kommen. Während des Prozesses musst Du den Strom und die Zeit überwachen, um sicherzustellen, dass die gewünschte Dicke der Nickelbeschichtung erreicht wird. Nach Abschluss des Prozesses müssen die Teile gründlich gespült und getrocknet werden. Es ist wichtig, alle Sicherheitsvorkehrungen zu beachten und geeignete Schutzausrüstung zu tragen, um Verletzungen zu vermeiden. Mit dieser Schritt-für-Schritt-Anleitung kannst Du nun erfolgreich Deine eigenen galvanisch vernickelten Teile herstellen.
5. Tipps und Tricks, um das bestmögliche Ergebnis zu erzielen
Um das bestmögliche Ergebnis beim galvanischen Vernickeln zu erzielen, gibt es einige Tipps und Tricks, die du beachten solltest. Zunächst einmal ist es wichtig, dass du alle notwendigen Materialien und Werkzeuge bereitstellst, bevor du mit dem Prozess beginnst. Eine sorgfältige Vorbereitung ist der Schlüssel zum Erfolg. Außerdem solltest du darauf achten, dass die zu vernickelnde Oberfläche gründlich gereinigt und entfettet ist, um eine optimale Haftung des Nickelüberzugs zu gewährleisten. Eine gleichmäßige Stromzufuhr und eine angemessene Dauer des galvanischen Bades sind ebenfalls entscheidend für ein perfektes Ergebnis. Wenn du diese Tipps und Tricks befolgst, wirst du mit Sicherheit ein großartiges Ergebnis erzielen und deine DIY-Projekte auf eine neue Ebene bringen.
6. Anwendung des galvanischen Vernickelns
Wenn Du Dich fragst, wofür das galvanische Vernickeln verwendet wird, dann bist Du hier genau richtig. Das galvanische Vernickeln ist eine Methode, um Metallgegenstände mit einer dünnen Nickelschicht zu überziehen. Diese Schicht schützt das Metall vor Korrosion und verleiht ihm eine glänzende Oberfläche. Das galvanische Vernickeln wird in vielen Bereichen eingesetzt, wie zum Beispiel in der Elektronikindustrie, der Automobilindustrie und der Schmuckherstellung. Es ist eine kostengünstige Methode, um Metallgegenstände zu veredeln und sie vor äußeren Einflüssen zu schützen. Mit unserem DIY-Tutorial kannst Du das galvanische Vernickeln ganz einfach zu Hause durchführen und Deine eigenen Metallgegenstände veredeln.
7. Wichtige Dinge, die man beachten muss, wenn man galvanisch vernickelt
Wenn Du Dich dazu entschieden hast, galvanisch zu vernickeln, gibt es einige wichtige Dinge, die Du beachten solltest, um ein optimales Ergebnis zu erzielen. Zunächst einmal ist es wichtig, dass das zu vernickelnde Objekt sauber und frei von Öl, Fett und anderen Verunreinigungen ist. Eine gründliche Reinigung mit einem geeigneten Reinigungsmittel ist daher unerlässlich. Zudem solltest Du darauf achten, dass die Stromstärke und die Dauer des Galvanisierungsprozesses auf das Material und die Größe des zu vernickelnden Objekts abgestimmt sind. Eine zu hohe Stromstärke oder eine zu lange Galvanisierungszeit können zu unerwünschten Ergebnissen führen. Schließlich solltest Du auch darauf achten, dass Du alle notwendigen Sicherheitsvorkehrungen einhältst, um Verletzungen oder Schäden zu vermeiden. Mit diesen wichtigen Tipps und ein wenig Übung kannst Du jedoch erfolgreich galvanisch vernickeln und Deine Objekte mit einer langlebigen und attraktiven Nickelschicht versehen.
8. Was sind die Vor- und Nachteile der galvanischen Vernickelung?
Wenn du dich dazu entscheidest, galvanisch zu vernickeln, gibt es einige Vor- und Nachteile, die du berücksichtigen solltest. Der größte Vorteil ist die Schutzfunktion, die die Vernickelung bietet. Durch die galvanische Vernickelung wird das Basismetall vor Korrosion und Verschleiß geschützt. Außerdem kann die Vernickelung das Erscheinungsbild des Objekts verbessern und ihm ein glänzendes Aussehen verleihen. Allerdings gibt es auch einige Nachteile. Zum einen kann die Vernickelung teuer sein, insbesondere wenn sie von einem Fachmann durchgeführt wird. Zum anderen kann es schwierig sein, eine gleichmäßige Schicht aufzutragen, was zu ungleichmäßigen Ergebnissen führen kann. Außerdem kann die Vernickelung allergische Reaktionen auslösen, wenn das Objekt in Kontakt mit der Haut kommt. Trotzdem ist die galvanische Vernickelung eine beliebte Methode, um Metallgegenstände zu schützen und zu verschönern.
9. Welche Kosten kann ein DIY-Projekt verursachen?
Wenn Du Dich dazu entscheidest, galvanisch zu vernickeln, solltest Du Dir bewusst sein, dass es einige Kosten verursachen kann. Zunächst benötigst Du eine geeignete Stromquelle, wie beispielsweise ein Netzgerät, das auf die benötigte Spannung und Stromstärke eingestellt werden kann. Außerdem benötigst Du eine Nickel-Elektrolytlösung, die je nach Größe des zu vernickelnden Objekts unterschiedlich viel kostet. Auch das Zubehör wie Anoden, Kathoden und Verbindungskabel müssen berücksichtigt werden. Darüber hinaus benötigst Du geeignete Schutzkleidung, um Dich vor den Chemikalien zu schützen. Wenn Du das gesamte Equipment selbst kaufst, kann es schnell teuer werden. Allerdings gibt es auch die Möglichkeit, sich das Equipment auszuleihen oder in einem DIY-Shop zu mieten. Es ist wichtig, dass Du Dir im Vorfeld überlegst, ob sich die Kosten für das DIY-Projekt lohnen und ob Du das Equipment auch in Zukunft nutzen wirst.
10. Fazit: Galvanische Vernickelung als eine effiziente Möglichkeit, Metalloberflächen zu schützen
Wenn es darum geht, Metall zu schützen, ist die galvanische Vernickelung eine äußerst effiziente Methode. Durch das Aufbringen einer dünnen Nickelschicht auf die Metalloberfläche wird diese vor Korrosion und Abrieb geschützt. Außerdem verleiht die Vernickelung dem Metall ein glänzendes und ansprechendes Aussehen. Das Beste daran ist, dass du die galvanische Vernickelung ganz einfach selbst durchführen kannst. Mit ein paar grundlegenden Werkzeugen und Materialien kannst du deine eigenen Metallteile vernickeln und ihnen damit eine längere Lebensdauer und ein besseres Aussehen verleihen. Ob du nun ein Hobbybastler oder ein professioneller Handwerker bist, die galvanische Vernickelung ist definitiv eine Fertigkeit, die sich lohnt zu erlernen.
- Kann Nickel direkt auf Messing abgeschieden werden?
-
Ja. Nickel kann galvanisch direkt auf Messing abgeschieden werden. Für einen sicheren Start empfiehlt sich ein kurzer Nickel-Strike (sauer, chloridreich) als Zwischenlage; danach wird mit Nickel aufgebaut.
Empfohlene Prozessfolge
- Entfetten, gründlich spülen.
- Mikrobeize für Cu/Zn-Legierungen (sehr kurz), spülen.
- Saure Aktivierung (Konditionierer), nass-zu-nass weiter.
- Nickel-Strike, Start bei niedriger Stromdichte, 20–90 s.
- anschließend Nickel.
Hinweise
- Entzinkung vermeiden: Beiz-/Aktivierungszeiten kurz halten; keine Trockenphasen.
- Startparameter: zunächst niedrige Stromdichte, dann zügig auf Sollwert erhöhen; ein moderater Chloridanteil fördert die Haftung.
- Gegen gelbliches Durchschlagen: ausreichende Ni-Gesamtdicke einplanen.
Typische Fehler & Abhilfe
- Blasen/Abblättern: Beize zu lang, Oberfläche verschmutzt, Startstrom zu hoch → Zeiten verkürzen, frisch aktivieren, mit niedriger Stromdichte starten.
- Dunkelgrauer Anlauf/Passivierung: Wartezeiten vermeiden, Aktivierung erneuern.
- Rauheit: Filtration/Spülqualität verbessern, Partikelquellen ausschließen.
- Muss man nach dem Verzinken passivieren?
-
Ob eine Passivierung nach dem Verzinken notwendig ist, hängt vom Verwendungszweck und den Anforderungen ab.
Nicht immer zwingend erforderlich
Für viele Standardanwendungen ist eine reine Zinkschicht (z. B. durch Feuerverzinken oder galvanisches Verzinken) ausreichend, um einen Basisschutz vor Korrosion zu gewährleisten. Insbesondere bei Bauteilen, die keinen besonders hohen optischen oder korrosiven Ansprüchen ausgesetzt sind, wird oft auf eine Passivierung verzichtet.
Vorteile der Passivierung
- Zusätzlicher Korrosionsschutz: Passivierungen (z. B. Chromatieren in verschiedenen Farben, Phosphatieren etc.) erzeugen eine zusätzliche Schutzschicht, die das darunterliegende Zink vor Oxidation bewahrt und die Lebensdauer erhöht.
- Bessere Optik: Passivierte Oberflächen können je nach Verfahren (blau, gelb, schwarz etc.) optisch aufgewertet werden.
- Reduzierung von Weißrost: Gerade bei frisch verzinkten Oberflächen kann es zu „Weißrost“ kommen, wenn sie Feuchtigkeit oder Kondenswasser ausgesetzt sind. Eine Passivierung verringert dieses Risiko.
Spezielle Anforderungen
Bei Bauteilen, die extremen Umweltbedingungen (z. B. Salzsprühnebel, hohe Luftfeuchtigkeit oder aggressive Chemikalien) ausgesetzt sind oder eine definierte Optik erfordern (wie in der Automobilindustrie oder bei dekorativen Anwendungen), ist eine Passivierung bzw. Chromatierung in der Regel empfehlenswert oder sogar vorgeschrieben.
Fazit
Eine Passivierung nach dem Verzinken ist nicht in jedem Fall obligatorisch, bringt jedoch klare Vorteile in Bezug auf Korrosionsschutz und Optik. Ob sie erforderlich ist, hängt von den jeweiligen Einsatzbedingungen und Qualitätsanforderungen ab.
- Gelbchromatieren - gelb verzinken
-
Unter Gelbchromatieren (umgangssprachlich auch „gelb verzinken“ genannt) versteht man ein Verfahren aus der Galvanotechnik, bei dem bereits verzinkte Oberflächen durch eine gelbe Passivierung weiterveredelt werden. Das Resultat ist eine charakteristische gelbliche bis goldene Oberfläche, die sowohl ästhetisch als auch korrosionshemmend ist.
Wie funktioniert Gelbchromatieren?
-
Zinkschicht als Basis
Zunächst wird das Metall (z. B. Stahl) verzinkt, entweder durch galvanisches Verzinken oder Feuerverzinken. Diese Zinkschicht bildet die Grundlage für das Chromatierverfahren.
-
Chemische Nachbehandlung
Im Anschluss erfolgt eine Passivierung oder Chromatierung. Bei der gelben Variante entsteht während dieses Prozesses durch eine spezielle Chromatlösung der typische gelbe bis goldene Farbton.- Früher wurde oft Chrom(VI) verwendet, das jedoch heute weitgehend reglementiert ist.
- Moderne Systeme basieren zunehmend auf Chrom(III), um Umwelt- und Gesundheitsauflagen zu erfüllen.
-
Farbentwicklung
Die Zinkoberfläche reagiert mit den Inhaltsstoffen der Chromatlösung und bildet eine Konversionsschicht („Chromatschicht“). Diese verstärkt den Korrosionsschutz und erzeugt den typischen gelb-goldenen Farbton.
Warum Gelbchromatieren?
- Optische Aufwertung: Die gelbe/goldene Oberfläche ist dekorativ und in vielen Branchen gefragt, etwa für Beschläge, Schrauben oder Zierteile.
- Zusätzlicher Korrosionsschutz: Die Chromatschicht schützt das darunterliegende Zink weiter vor Oxidation.
- Bewährter Standard: Gelbchromatierte Teile gelten seit Jahrzehnten als Referenz für korrosionsbeständige, optisch ansprechende Oberflächen.
Chrom(VI)-frei vs. Chrom(VI)-haltig
- Chrom(VI)-haltig: Verbreitete ältere Verfahren. Intensiv gelbe Färbung, jedoch stark reguliert oder verboten aufgrund der schädlichen Auswirkungen auf Umwelt und Gesundheit.
- Chrom(III)-basiert: Deutlich umwelt- und gesundheitsverträglicher, die Farbintensität kann etwas weniger ausgeprägt sein, dafür entsprechen diese Verfahren aktuellen Auflagen und entwickeln sich stetig weiter.
Vorteile und Grenzen des Gelbchromatierens
Vorteile
- Markante gelbe/goldene Optik
- Zusätzlicher Korrosionsschutz gegenüber rein verzinkten Oberflächen
- Vielseitig einsetzbar, z. B. in der Automobilindustrie, Elektronik oder im Haushalt
Nachteile
- Umweltauflagen bei Chrom(VI)-haltigen Prozessen
- Beschränkung auf Gelb-/Goldtöne
- Qualität stark abhängig von der Vorbehandlung und Beschaffenheit der Zinkschicht
Fazit
Gelbchromatieren ist eine Nachbehandlung verzinkter Oberflächen, durch die eine gelbe bzw. goldene Chromatschicht entsteht. Diese Schicht verstärkt den Korrosionsschutz und verleiht dem Werkstück ein charakteristisches gelb/goldenes Aussehen. Früher vorrangig mit Chrom(VI)-haltigen Lösungen durchgeführt, kommen heute immer öfter Chrom(III)-basierte Systeme zum Einsatz, um Umwelt- und Gesundheitsauflagen gerecht zu werden. Trotz gewisser Unterschiede hinsichtlich der Farbintensität oder der Prozessführung gehören gelbchromatierte Oberflächen nach wie vor zu den beliebtesten und verbreitetsten Varianten in der Galvanik.
-
Zinkschicht als Basis
- Schwarzchromatieren – Schwarz verzinken
-
Unter Schwarzchromatieren (umgangssprachlich auch als „schwarz verzinken“ bezeichnet) versteht man ein Verfahren aus der Galvanotechnik, bei dem eine bereits verzinkte Oberfläche durch eine spezielle dunkle Passivierung weiterbehandelt wird. Diese chemische Nachbehandlung erzeugt eine tiefschwarze bzw. anthrazitfarbene Chromatschicht, die sowohl den Korrosionsschutz verbessert als auch eine markante dunkle Optik verleiht.
Wie funktioniert Schwarzchromatieren?
-
Zinkschicht als Grundlage
Zu Beginn wird das Metall (z. B. Stahl) verzinkt (galvanisch oder durch Feuerverzinken), sodass eine Zinkschicht als Basisschutz vorhanden ist.
-
Dunkle Passivierung
Nach dem Verzinken erfolgt die Passivierung/Chromatierung mit einer speziellen Lösung, die durch ihre Zusammensetzung eine schwarze Einfärbung bewirkt. Traditionell standen dafür chrom(VI)-haltige Lösungen zur Verfügung, die jedoch aufgrund gesundheitlicher und umweltrechtlicher Bestimmungen stark reglementiert sind. Moderne chrom(III)-basierte oder andere chrom(VI)-freie Verfahren haben sich mittlerweile etabliert und bieten eine sehr dunkle Oberfläche.
-
Reaktion und Schichtbildung
In der Passivierungslösung reagiert die vorhandene Zinkschicht mit bestimmten Chemikalien. Es bildet sich eine Konversionsschicht (Chromatschicht), die schwarz gefärbt ist und einen zusätzlichen Schutz vor Korrosion bewirkt.
Vorteile und Anwendungsgebiete
- Markante Optik: Die schwarze Oberfläche ist aus Design- oder Tarnungsgründen (z. B. bei militärischen Anwendungen) beliebt.
- Erweiterter Korrosionsschutz: Die Chromatschicht schützt das darunterliegende Zink vor Oxidation und verlängert damit die Lebensdauer.
- Vielseitige Einsatzmöglichkeiten: Schwarzchromatierte Teile finden sich in der Automobilindustrie, bei Schrauben und Befestigungselementen, in der Elektronik, im Heimwerkerbereich und in dekorativen Anwendungen.
Chrom(VI)-basierte versus chrom(VI)-freie Systeme
- Chrom(VI)-haltige Verfahren: Lieferten eine intensiv schwarze Färbung, sind aber aus Umwelt- und Gesundheitsgründen (z. B. REACH-Verordnung) stark eingeschränkt oder verboten.
- Chrom(VI)-freie/chrom(III)-basierte Systeme: Bieten eine dunkle Einfärbung, schonen Umwelt und Gesundheit und werden stetig weiterentwickelt, um hinsichtlich Farbintensität und Korrosionsschutz mit den früheren Verfahren zu konkurrieren.
Grenzen des Schwarzchromatierens
- Anfälligkeit bei starker Beanspruchung: Mechanische Belastungen (z. B. Reibung, Kratzer) können die dunkle Chromatschicht abnutzen.
- Prozessgenauigkeit: Damit das Ergebnis einheitlich schwarz wird, müssen Bäder und Prozessparameter (Temperatur, Zeit, Chemikalien) genau eingehalten werden.
- Abhängigkeit von der Zinkqualität: Eine gute Zinkschichtvorbehandlung ist essenziell, da die Schwarztönung nur gut haftet, wenn das Zink sauber und gleichmäßig abgeschieden wurde.
Fazit
Schwarzchromatieren, häufig auch als „schwarz verzinken“ bezeichnet, ist ein Verfahren zur dunklen Passivierung verzinkter Oberflächen. Das Resultat ist ein tiefschwarzes bzw. dunkles Erscheinungsbild und eine zusätzliche Steigerung des Korrosionsschutzes. In chrom(VI)-freien Varianten stellt Schwarzchromatieren heute eine umwelt- und gesundheitsschonendere Möglichkeit dar, eine attraktive, schwarze Oberfläche zu erzeugen.
-
Zinkschicht als Grundlage
- Selber galvanisch verzinken: Ein Leitfaden zum einfachen DIY-Projekt!
-
DIY-Liebhaber aufgepasst: Selber galvanisch verzinken ist einfacher als gedacht! Mit unserer Anleitung erhaltet ihr einen ausführlichen Überblick über die Grundlagen des Verzinkens und die Vorteile, die es mit sich bringt. Auf geht's zu einem spannenden DIY-Projekt!
1. Einleitung
Hey, du! Möchtest du lernen, wie du deine eigenen Metallteile galvanisch verzinken kannst? Dann bist du hier genau richtig! In diesem Leitfaden zeigen wir dir Schritt für Schritt, wie du dein DIY-Projekt umsetzen kannst. Doch bevor wir loslegen, möchten wir dir erklären, was galvanisches Verzinken überhaupt bedeutet. Dabei handelt es sich um ein Verfahren, bei dem eine Schutzschicht auf das Metall aufgetragen wird, um es vor Korrosion zu schützen. Diese Schutzschicht besteht aus Zink und wird durch eine chemische Reaktion auf das Metall aufgebracht. Nun weißt du, was dich erwartet – lass uns loslegen!
2. Was ist Galvanisches Verzinken?
Galvanisches Verzinken ist ein Prozess, bei dem eine Schicht aus Zink auf ein Metall aufgetragen wird, um es vor Korrosion zu schützen. Es ist eine der am häufigsten verwendeten Methoden zum Schutz von Stahl und Eisen gegen Rost. Der Prozess funktioniert durch Elektrolyse, bei der das Metall in eine Zinklösung getaucht wird und eine elektrische Ladung durch das Metall geleitet wird. Dies führt dazu, dass das Zink aus der Lösung auf das Metall aufgetragen wird, wodurch eine Schutzschicht entsteht. Galvanisches Verzinken ist eine kostengünstige und effektive Methode, um Metalle vor Korrosion zu schützen und ist auch für DIY-Projekte geeignet. Mit einigen grundlegenden Kenntnissen und Werkzeugen kannst Du Deine eigenen galvanischen Verzinkungsprojekte zu Hause durchführen.
3. Vorbereitungen treffen
Bevor du mit dem galvanischen Verzinken beginnst, solltest du einige Vorbereitungen treffen, um ein erfolgreiches DIY-Projekt zu gewährleisten. Zunächst solltest du sicherstellen, dass du alle notwendigen Materialien und Werkzeuge zur Hand hast, wie zum Beispiel einen Zinkanoden, ein Verzinkungsbad, eine Stromquelle und Schutzhandschuhe. Es ist auch wichtig, dass du einen geeigneten Arbeitsplatz einrichtest, der gut belüftet ist und keine brennbaren Materialien in der Nähe hast. Bevor du mit dem Verzinkungsprozess beginnst, musst du sicherstellen, dass das zu verzinkende Objekt gründlich gereinigt und entfettet ist, um eine optimale Haftung der Zinkschicht zu gewährleisten. Vergiss nicht, dass Sicherheit an erster Stelle steht und du immer Schutzhandschuhe und eine Schutzbrille tragen solltest, um Verletzungen zu vermeiden. Mit diesen Vorbereitungen bist du bereit, dein DIY-Projekt des galvanischen Verzinkens erfolgreich umzusetzen.
4. Werkzeug und Materialien zum Galvanisieren besorgen
Um dein DIY-Projekt des galvanischen Verzinkens erfolgreich durchzuführen, benötigst du die richtigen Werkzeuge und Materialien. Zunächst solltest du dich für eine geeignete Verzinkungslösung entscheiden, die du bei uns erwerben kannst. Auch ein geeigneter Behälter, in dem du das Verzinkungsbad anmischen und das zu verzinkende Objekt eintauchen kannst, ist von großer Bedeutung. Hier eignet sich beispielsweise ein Kunststoffbehälter oder ein alter Topf aus Edelstahl. Ein weiteres wichtiges Werkzeug ist ein Gleichrichter, der die Stromstärke reguliert und somit ein gleichmäßiges Verzinkungsergebnis ermöglicht. Zudem benötigst du eine Anode, die aus Zink besteht und in das Verzinkungsbad gehängt wird. Diese dient als Stromquelle und sorgt dafür, dass sich das Zink auf dem zu verzinkenden Objekt ablagert. Um das Objekt vor dem Verzinken gründlich zu reinigen, empfiehlt sich die Verwendung von Schleifpapier und Reinigungsmitteln wie beispielsweise Isopropanol. Mit diesen Werkzeugen und Materialien bist du bestens gerüstet, um dein DIY-Projekt des galvanischen Verzinkens erfolgreich umzusetzen.
5. Die Oberfläche vorbereiten und einfetten
Bevor du mit dem eigentlichen Verzinkungsprozess beginnen kannst, musst du sicherstellen, dass die Oberfläche des zu verzinkenden Objekts glatt und sauber ist. Dazu solltest du es gründlich reinigen und gegebenenfalls von Rost befreien. Anschließend solltest du die Oberfläche mit einer Drahtbürste oder Schleifpapier leicht anrauen, um eine bessere Haftung der Zinkschicht zu gewährleisten. Um ein optimales Ergebnis zu erzielen, ist es außerdem ratsam, die Oberfläche vor dem Verzinken mit einem geeigneten Fett oder Öl zu behandeln. Dadurch wird verhindert, dass das Zink an unerwünschten Stellen haftet und es entstehen keine unschönen Tropfen oder ungleichmäßige Schichten. Achte darauf, dass du nur spezielle Fette oder Öle verwendest, die für den Verzinkungsprozess geeignet sind. Mit einer gründlichen Vorbereitung der Oberfläche und einer sorgfältigen Behandlung mit Fett oder Öl steht dem erfolgreichen DIY-Projekt nichts mehr im Wege.
6. Das galvanische Verzinken durchführen
Bevor du mit dem galvanischen Verzinken beginnst, solltest du sicherstellen, dass du alle notwendigen Materialien und Werkzeuge zur Hand hast. Dazu gehören unter anderem ein Zinkanoden-Set, ein Gleichstromnetzteil, ein Kunststoffbehälter, einen Zinkelektrolyt und Handschuhe zum Schutz vor Chemikalien. Zunächst musst du das zu verzinkende Objekt gründlich reinigen und entfetten, um eine optimale Haftung der Zinkschicht zu gewährleisten. Anschließend wird das Objekt als Kathode an das Gleichstromnetzteil angeschlossen und in den Zinkelektrolyt getaucht. Die Zinkanode dient als Anode und gibt Zinkionen ab, die sich auf dem Objekt abscheiden und eine Schutzschicht bilden. Je länger das Objekt im Elektrolyt bleibt, desto dicker wird die Zinkschicht. Nach dem Verzinken sollte das Objekt gründlich abgespült und getrocknet werden. Mit etwas Übung und Geduld kannst du so auch zu Hause eine professionelle Verzinkung durchführen.
7. Nachbehandlung der Teile nach dem Verzinken
Nachdem Du erfolgreich Deine Teile verzinkt hast, ist es wichtig, sie richtig nachzubehandeln, um ihre Haltbarkeit und Ästhetik zu gewährleisten. Zunächst solltest Du die Teile gründlich mit Wasser abspülen, um überschüssige Zinkreste zu entfernen. Anschließend kannst Du sie mit einem milden Reinigungsmittel und einem weichen Tuch reinigen, um eventuelle Schmutzrückstände zu entfernen. Danach solltest Du die Teile gründlich trocknen lassen, bevor Du sie mit einer Schutzschicht versiegelst. Hierfür eignet sich ein spezielles Spray oder eine Versiegelung aus Wachs oder Öl. Die Schutzschicht schützt die Teile vor Korrosion und verleiht ihnen eine glänzende Optik. Beachte jedoch, dass die Nachbehandlung je nach Art der Teile und der Verzinkung variieren kann. Informiere Dich daher im Vorfeld über die empfohlenen Schritte für Dein spezielles Projekt.
8. Fehler beim Selber-Galvanisieren vermeiden
Wenn Du Dich entscheidest, Dein DIY-Projekt mit einer galvanischen Verzinkung zu veredeln, solltest Du einige Fehler vermeiden, um das bestmögliche Ergebnis zu erzielen. Ein häufiger Fehler ist die ungenügende Reinigung des zu verzinkenden Gegenstandes. Es ist wichtig, dass alle Fett- und Ölrückstände entfernt werden, da diese die Haftung der Zinkschicht beeinträchtigen können. Auch das Entfernen von Rost und anderen Verunreinigungen ist ein wichtiger Schritt, um eine gleichmäßige und haltbare Zinkschicht zu erzielen. Ein weiterer Fehler ist die ungenügende Vorbereitung der Elektrolytlösung. Es ist wichtig, die richtigen Mengen an Zink- und Salzsäure zu verwenden, um eine optimale Leitfähigkeit zu gewährleisten. Auch die Wahl des richtigen Stromstärke ist entscheidend, um eine gleichmäßige Zinkschicht zu erzielen. Wenn Du diese Fehler vermeidest, kannst Du sicher sein, dass Dein DIY-Projekt mit einer galvanischen Verzinkung ein voller Erfolg wird.
9. Fazit: Selber galvanisch verzinken – ein lohnendes DIY-Projekt!
Fazit: Selber galvanisch verzinken – ein lohnendes DIY-Projekt! Zusammenfassend lässt sich sagen, dass das selber galvanisch verzinken ein lohnendes DIY-Projekt ist. Es ist nicht nur kostengünstiger als das Beauftragen eines professionellen Dienstleisters, sondern auch eine tolle Möglichkeit, sich mit der Technik des Verzinkens vertraut zu machen. Mit ein wenig Übung und Geduld können auch Einsteiger schnell gute Ergebnisse erzielen. Wichtig ist jedoch, die nötigen Sicherheitsvorkehrungen zu treffen und sich an die Anleitung zu halten. Wer also auf der Suche nach einem neuen DIY-Projekt ist und sich für Metallverarbeitung interessiert, sollte das galvanische Verzinken auf jeden Fall ausprobieren.
- Wie kann man auf Zink (auch Zamak) beschichten?
-
Galvanische Beschichtung auf Zink oder Zinkdruckguss
Wenn bereits Zink (z. B. Zinkdruckguss oder verzinkte Oberflächen) als Substrat vorhanden ist und darauf eine weitere galvanische Schicht (z. B. Kupfer, Nickel, Chrom etc.) aufgetragen werden soll, gelten etwas andere Anforderungen als bei Stahl. Zink ist ein relativ reaktives Metall und kann in starken Säuren oder Laugen schnell angegriffen werden. Außerdem neigt es zur Oxidbildung, die eine gute Haftung erschweren kann. Typischerweise wird daher – insbesondere bei Zinkdruckguss – ein sogenannter „Strike“ (Haftvermittler-Schicht) eingesetzt, um eine zuverlässige Haftung für die darauffolgende Deckschicht zu gewährleisten. Als Haftvermittlerschicht (Strike) wird ein alkalischer Kupferelektrolyt verwendet.
Nachfolgend eine empfohlene Prozessabfolge, wenn auf Zink oder Zinkdruckguss galvanisch beschichtet werden soll:
-
Reinigen / Entfetten
Zweck: Entfernung von Fetten, Ölen und sonstigen Verunreinigungen.
Hinweise: Geeignete (milde) Reiniger verwenden, da Zink in stark alkalischen Medien angegriffen werden kann. Meist Tauchbad-Verfahren, ggf. unterstützt durch Ultraschall oder Spritzreinigung. -
Spülen
Zweck: Beseitigung von Reinigerresten, um kein Verschleppen in nachfolgende Bäder zu riskieren.
Tipp: Häufig sind mehrstufige Spülungen (kaltes oder warmes Wasser) sinnvoll, um die Oberfläche vollständig zu säubern. -
Leichtes Beizen / Aktivieren (Konditionierer)
Zweck: Entfernen dünner Oxidschichten und Aktivieren der Zinkoberfläche.
Konditionierer: Spezielles, mildsaures Bad, das leicht verdünnt (gemäß Herstellerangaben) angesetzt wird. So wird die Zinkoberfläche schonend behandelt, ohne sie übermäßig anzugreifen. -
Kurzspülen
Zweck: Entfernen von Beiz- bzw. Konditionierer-Rückständen, um die nachfolgenden Bäder nicht zu verunreinigen.
-
Haftvermittler-Schicht (alkalischer Kupferelektrolyt)
Zweck: Aufbringen einer sehr dünnen, aber haftstarken Metallschicht als Basis für die folgenden Beschichtungen.
Alkalischer Kupferelektrolyt:
- Liefert eine gute Haftung auf Zink, sofern die Oberfläche korrekt vorbereitet ist.
- Ist (im Vergleich zu cyanidhaltigen Bädern) umweltfreundlicher und sicherer. -
Haupt-Beschichtung
Optionen:
- Weitere Kupferschicht (sauer) für Leitfähigkeit und Glättung.
- Nickel für Korrosionsschutz und Härte.
- Chrom (nach Nickel) für Glanz und Verschleißbeständigkeit.
- Andere Metalle oder Legierungen (z. B. Messing, Zinn, Bronze) je nach Bedarf. -
Spülen / Nachbehandlung
Zweck: Entfernung von Elektrolytresten und Additiven.
Optional: Passivierung oder Versiegelung für zusätzlichen Korrosionsschutz oder spezielle Optik. -
Trocknen / Endkontrolle
Trocknung: Zentrifuge, Warmluftofen oder ähnliche Verfahren, um Wasserflecken zu vermeiden.
Abschluss: Sichtprüfung, Messung der Schichtdicke und Haftfestigkeits-Tests.
Kurzfassung der Prozessschritte
- Entfetten / Reinigen
- Spülen
- Leichtes Beizen / Aktivieren (Konditionierer, verdünnt)
- Spülen
- Haftvermittlerschicht (alkalischer Kupferelektrolyt)
- Haupt-Beschichtung (z. B. Glanzkupfer, Nickel)
- Spülen / Nachbehandlung
- Trocknen / Endkontrolle
-
- Das Netzteil zeigt nix an, oder erreicht nicht die Spannung
-
Die Netzteile regeln den Stromfluss über die Spannung, dies ergibt sich aus dem Ohmschen Gesetz. Wenn kein Verbraucher angeschlossen ist, kann auch kein Strom fließen.
Sollte die Strombegrenzung auf Null gestellt sein, wird auch die Spannung auf 0 abfallen.
Spannung einstellen
- Drehe den Spannungs-Grob- und Feinregler bis die gewünschte Ausgangsspannung auf dem Display angezeigt wird
- Achte darauf, dass die eigestellte Spannung nicht die maximale Versorgungsspannung des zu betreibenden Verbrauchers überschreitet
- Sollte sich die Spannung nicht weiter erhöhen lassen, ist wahrscheinlich die Strombegrenzung zu niedrig eingestellt, erhöhe diese
- Der Stromfluss ergibt sich dann mit dem ohmschen Widerstand
Strombegrenzung einstellen
- Stelle eine sehr niedrige Spannung von ca. 1 V- ein, um Funkenbildung zu vermeiden, und bilde mit angeschlossenen Messleitungen einen Kurzschluss
- Daraufhin wechselt das Netzgerät vom Konstantspannungs-Modus in den Konstantstrom-Modus (Im Display wird C.C anstelle von C.V angezeigt)
- Drehe jetzt den Strom-Grob- und Feinregler bis der gewünschte Ausgangsstrom auf dem Display angezeigt wird
- Nachdem die Strombegrenzung erfolgreich eingestellt wurde, kann der Kurzschluss wieder gelöst werden
- Erhöhe anschließend die Spannung wieder auf den gewünschten Wert
- Wenn du mit der Strombegrenzung arbeitest, wird die Spannung entsprechend dem angelegten Widerstand reduziert
Sollte kein Strom fließen ist die Kontaktierung zu prüfen.
- Es bildet sich schwarzer Schlamm oder die Abscheidung wird matt
-
Wenn sich bei der Galvanik schwarzer Schlamm bildet oder die Beschichtung matt wird, kann dies auf mehrere Probleme im Galvanikprozess hinweisen. Hier sind die häufigsten Ursachen:
Überschüssiger Strom (Überstrom):
- Symptom: Bildung von schwarzem Schlamm oder eine matte, ungleichmäßige Oberfläche.
- Ursache: Wenn der Strom zu hoch eingestellt ist, können sich Metallpartikel zu schnell abscheiden, was zu einer grobkörnigen, porösen oder sogar schwarzen Ablagerung führt. Dies ist besonders häufig, wenn die Stromdichte (Strom pro Fläche) zu hoch ist.
- Lösung: Reduziere den Strom oder die Spannung, um eine gleichmäßigere und glattere Metallabscheidung zu erreichen (beachte aber, dass es bei manchen Elektrolyten auch sein kann, dass die Schicht matt wird, wenn die Stromdichte zu niedrig ist).
Schlechte Reinigung des Werkstücks:
- Symptom: Unregelmäßige, matte Beschichtung oder schwarze Flecken.
- Ursache: Verunreinigungen, Oxidation oder Fett auf der Oberfläche des Werkstücks können die ordnungsgemäße Metallabscheidung stören und zu Defekten in der Beschichtung führen.
- Lösung: Reinige das Werkstück gründlich, bevor du es in das Elektrolytbad tauchst. Entferne alle Fette, Oxidschichten und Verschmutzungen durch gründliches Waschen, Schleifen und Spülen.
Ungeeignetes Werkstückmaterial:
- Symptom: Schwarzer Schlamm im Elektrolyt oder eine matte Beschichtung.
- Ursache: Wenn das Werkstückmaterial nicht für den verwendeten Elektrolyten geeignet ist, kann es sich auflösen und den Elektrolyten verunreinigen. Dies führt zu einer schlechteren Beschichtung und unerwünschten Ablagerungen.
- Lösung: Stelle sicher, dass das Werkstückmaterial kompatibel mit dem verwendeten Elektrolyten ist. Überprüfe die Materialzusammensetzung und wähle einen geeigneten Elektrolyten, um chemische Reaktionen, die zur Verunreinigung führen, zu vermeiden.
Unzureichende Elektrodenführung:
- Symptom: Schwarze Ablagerungen in bestimmten Bereichen.
- Ursache: Eine ungleichmäßige Stromverteilung durch schlechte Positionierung der Anode oder Kathode kann dazu führen, dass an einigen Stellen zu viel Metall abgeschieden wird, was zu schwarzem Schlamm führt.
- Lösung: Stelle sicher, dass die Elektroden richtig positioniert und der Strom gleichmäßig verteilt ist. Überprüfe die Abstände zwischen den Elektroden und die Position des Werkstücks im Bad.
Zu lange Galvanisierdauer:
- Symptom: Matte oder dunkle Beschichtung.
- Ursache: Wenn das Werkstück zu lange im Elektrolytbad bleibt, kann es zu einer Übersättigung kommen, was zu einer matten oder sogar schwarzen Schicht führen kann.
- Lösung: Verkürze die Galvanisierzeit und überwache den Prozess regelmäßig, um sicherzustellen, dass die gewünschte Schichtdicke erreicht wird, ohne die Oberfläche zu beeinträchtigen.
Zu hohe oder niedrige Temperatur des Elektrolyten:
- Symptom: Mattheit oder schwarze Ablagerungen.
- Ursache: Temperaturabweichungen können die Geschwindigkeit der chemischen Reaktionen im Elektrolyten verändern, was die Qualität der Beschichtung beeinträchtigt.
- Lösung: Überprüfe und reguliere die Temperatur des Elektrolyten, um sicherzustellen, dass sie innerhalb des optimalen Bereichs für den spezifischen Galvanikprozess liegt.
Zusammenfassung:
Schwarzer Schlamm oder eine matte Beschichtung beim Galvanisieren sind meist das Ergebnis von zu hohem Strom, unzureichender Reinigung, ungeeignetem Werkstückmaterial, ungleichmäßiger Stromverteilung oder Temperaturproblemen. Durch die Anpassung dieser Parameter kann die Qualität der Beschichtung erheblich verbessert werden.
- Die Chromabscheidung wird dunkel
-
Es ist normal, dass Chrom in den ersten Phasen der Abscheidung dunkel erscheint. Das liegt daran, dass die Chromschicht anfangs sehr feinkristallin ist, wodurch das Licht anders reflektiert wird und die Oberfläche dunkel wirkt. Mit fortschreitender Abscheidung vergrößern sich die Kristalle, und die Schicht wird allmählich heller und nimmt die typische Chromfarbe an.
Es könnte auch sein, dass die Stromdichte zu hoch ist. Eine zu hohe Stromdichte führt dazu, dass sich die Chromschicht zu schnell und ungleichmäßig abscheidet, was ebenfalls zu einer dunklen oder schwarzen Oberfläche führen kann. Eine niedrigere Stromdichte sorgt für eine gleichmäßigere Kristallbildung und damit für eine hellere und gleichmäßigere Chromschicht. Hier muss ein Kompromiss aus Geschwindigkeit und Qualität gefunden werden.
Ein weiterer wichtiger Punkt ist, dass der Elektrolyt aufgrund der hohen Stromdichte zu warm wurde. Auch zu hohe Temperatur führt zur dunklen Färbung der Schicht. In diesem Fall müsste die Stromdichte verringert werden, oder die Abscheidung unterbrochen werden.
- Die Beschichtung auf Edelstahl hält nicht
-
Wenn die Beschichtung auf Edelstahl nicht haftet, liegt der Grund meist in einer unzureichenden Vorbehandlung. Edelstahl bildet beim Kontakt mit Luft innerhalb weniger Sekunden eine unsichtbare Oxidschicht, die das Metall vor chemischen Reaktionen schützt, jedoch auch die Haftung von Beschichtungen erheblich beeinträchtigt.
Um eine langlebige Beschichtung zu gewährleisten, ist es entscheidend, das Werkstück mit einem Nickel-Strike vorzubereiten. Dieser Galvano-Aktivator entfernt die Oxidschicht sowie das in der Edelstahllegierung enthaltene Chrom und bildet eine dünne, haftfähige Nickelschicht als Basis für die weitere Beschichtung.
Alternativ kann auch ein Gold-Strike (Gold-Flash) verwendet werden, um ähnliche Ergebnisse zu erzielen.
- Es scheidet sich kein Nickel auf Eisen ab
-
Es ist etwas Geduld nötig, da Nickel recht langsam abscheidet. Eventuell ist die Stromdichte zu niedrig, dann würde es viel länger dauern. Es sollten aber auch nicht zuviele Gasblasen entstehen, da sonst schwarze Streifen entstehen könnten.
Der große Nachteil ist, dass man die Nickelbildung auch sehr schlecht erkennen kann.
Kontrollieren Sie auch nochmal die Polarität der Anode, diese muss auf Plus sein, während der zu beschichtende Gegenstand auf Minus gepolt sein muss.
- Zahlungsmöglichkeiten
-
Bei uns kannst du deinen Kauf mit den folgenden Zahlungsmethoden abschließen:
- ApplePay
- Bancontact
- Belfius
- EPS
- KBC
- Klarna
- Kreditkarte
- PayPal
- Vorkasse (per Überweisung)
Die verfügbaren Zahlungsmethoden können je nach Lieferland, verwendeter Technik, gewählte Cookies oder Inhalt des Warenkorbes abweichen.
- Versandinformationen
-
Hier findest du die Versandkostentabelle.
Bei kleinen und leichten Dingen kann der Versand als Kleinpaket erfolgen (bis 1kg). Beachte aber, dass die Option "Kleinpaket" manchmal etwas länger dauert, bis diese zugestellt wird. Die Regellaufzeit in Deutschland beträgt 1 bis 4 Tage, in der EU meist ca. 3-7 Tage.
Land Paketversand Kleinpaket Deutschland (ohne Inseln) 7,00€ 3,50€ Belgien, Frankreich, Luxemburg, Österreich 12,00€ 6,90€ Liechtenstein, Schweiz 17,00€ 7,90€






































